Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C.
TN1: 150 ml dd Y (NaOH 2M) vào 100 ml dd X (AlCl3) à 7,8 gam kết tủa Al(OH)3
TN2: Thêm tiếp vào cốc trên 100 ml dd Y à 10,92 gam kết tủa Al(OH)3
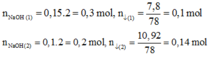



Đáp án A
• (1)0,3 mol NaOH + 0,1x mol AlCl3 → 0,1 mol Al(OH)3↓
(2)Thêm tiếp 0,2 mol NaOH → 0,14 mol Al(OH)3↓
→ Giai đoạn (1) kết tủa chưa tan; (2) kết tủa tan một phần
• 3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl (*)
Al(OH)3 + NaOHdư → NaAlO2 + 2H2O
Theo (*) nNaOH = 3 × nAlCl3 = 3 × 0,1x = 0,3x mol; nAl(OH)3 = 0,1x mol.
Theo (**) nAl(OH)3 phản ứng = 0,1x - 0,14 mol → nNaOH = 0,1x - 0,14 mol
→ ∑nNaOH = 0,3x + 0,1x - 0,14 = 0,3 + 0,2 → x = 1,6

Chọn đáp án C
● Gọi số mol NaOH dùng ở lần 1 là a mol ta có sơ đồ.
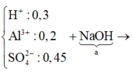
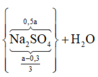
● ⇒ Với nNaOH = (a + 0,45) mol thì nAl(OH)3 = a - 0 , 3 6
+ Ta có sơ đồ:

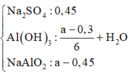
⇒ Ta có nAl(OH)3 = 4nAl(OH)3 – (nNaOH – nH+)
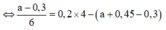
a = 0,6 mol ⇒ VNaOH = 0,6 lít = 600 ml ⇒ Chọn C

Đáp án D

Căn cứ vào bản chất phản ứng và giả thiết, ta có đồ thị sau :
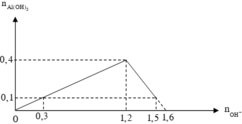
Dựa vào tính chất hình học của đồ thị, ta thấy :
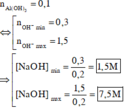

Đáp án D
2Al + 6H+ → 2Al3+ + 3H2
0,1 ←0,3 ← 0,15
[Al(OH)4]- + 4H+→ Al3+ + 4H2O
0,125 ← (0,8 – 0,3)
Al + OH- + 3H2O →[Al(OH)4]- + 3/2 H2
0,125 ← 0,125 ← 0,125
⇒ m = (0,125 + 0,1).27 = 6,075 g
⇒V dd NaOH = 0,125/ 2 = 0,0625 lít

Đáp án C
Dung dịch X + AgNO3 dư ⇒ mAgCl = 17,22 gam ⇒ nCl– = 0,12 mol.
+ Bảo toàn điện tích ⇒ nCu2+ = 0,01 mol.
+ Cho dung dịch X + 0,17 mol NaOH.
Tạo 0,04 mol Mg(OH)2 và 0,01 mol Cu(OH)2 tốn 0,1 mol NaOH.
+ Còn 0,07 mol NaOH tác dụng với Al3+.
⇒ nAl(OH)3↓ = 4nAl3+ – OH– = 0,02×4 – 0,07 = 0,01 mol.
⇒ m↓ = 0,04×58 + 0,01×98 + 0,01×78 = 4,08 gam
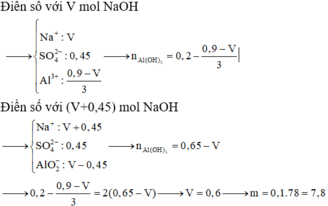

Đáp án B
Bản chất phản ứng là : Cho 340 ml dung dịch NaOH 1M vào cốc thủy tinh đựng 100 ml dung dịch AlCl 3 nồng độ x mol/lít, tạo ra 0,06 mol kết tủa. Ta có :
Suy ra đã có hiện tượng hòa tan kết tủa. Như vậy dung dịch sau phản ứng có chứa các ion Na + , Cl - và Al OH 4 - . Theo bảo toàn nguyên tố Cl, Al và bảo toàn điện tích, ta có :