
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



4.Viết PTHH cho mối chuyển đổi sau :
a) (1) CaO + CO2 \(\rightarrow CaCO_3\)
(2) CaCO3 \(\rightarrow\) CaO + CO2
(3) CaO + H2O \(\rightarrow\) Ca(OH)2
(4) CaO + HCl \(\rightarrow\) CaCl2 + H2O
b) (1) S + O2 \(\rightarrow\) SO2
(2) SO2 + Na2O \(\rightarrow\) Na2SO3
(3) Na2SO3 \(\rightarrow\) SO2 + Na2O
(4) SO2 + H2O \(\rightarrow\) H2SO3
![]() chúc bạn học tốt nha . #ah_kiêu
chúc bạn học tốt nha . #ah_kiêu ![]()

a/ PTHH: Zn + 2HCl ===> ZnCl2 + H2
b/ nZn = 16 / 65 = 0,25 mol
=> nH2 = nZn = 0,25 mol
=> VH2(đktc) = 0,25 x 22,4 = 5,6 lít
c/ nHCl = nZn = 0,25 mol
=> mHCl = 0,25 x 36,5 = 9,125 gam

(1) CH4 + 2O2 -to-> CO2 + 2H2O (2) 3Fe + 2O2 -to->Fe3O4 (3) 2Mg + O2 -to-> 2 MgO (7) 2KMnO4 -to-> K2MnO4 + MnO2 + O2 (8) Fe + 2HCl --> FeCl2 + H2 (9) HgO + H2 -to-> Hg + H2O | (4) 2KClO3 -to,MnO2--> 2KCl + 3O2 (5) SO3 + H2O --> H2SO4 (6) 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2 |
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2Fe+O_2\underrightarrow{t^o}2FeO\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)

a
đổ nước vào 3 lọ
nhúng QT vào 3 lọ
hóa đỏ => SO3 , P2O5
hóa xanh => Na2O
Cho BaCl2 vào các mẫu thử làm quỳ->đỏ:
Mẫu thử xh kết tủa trắng: H2SO4(SO3)
b)
đổ nước vào 3 lọ
nhúng QT vào 3 lọ
hóa xanh => Na2O
hóa đỏ => P2O5
k đổi màu => CaCO3
a.Trích một ít mẫu thử và đánh dấu:
Đưa nước có quỳ tím vào 3 mẫu thử:
-Na2O: quỳ hóa xanh
\(Na_2O+H_2O\rightarrow2NaOH\)
-SO3,P2O5: quỳ hóa đỏ
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
Nhỏ vài giọt dd BaCl2 vào:
-SO3: xuất hiện kết tủa trắng
\(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
-Còn lại là P2O5
b.Trích một ít mẫu thử và đánh dấu:
Cho 3 chất rắn vào nước có quỳ tím:
-CaCO3: không tan trong nước, quỳ không chuyển màu
-Na2O: quỳ hóa xanh
\(Na_2O+H_2O\rightarrow2NaOH\)
-P2O5: quỳ hóa đỏ
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)

\(PTK_x=2\cdot56+\left(32+16\cdot4\right)a=400\\ \Rightarrow96a=288\\ \Rightarrow a=3\)
Do đó CTHH \(X:Fe_2\left(SO_4\right)_3\)
Vì \(SO_4\left(II\right)\Rightarrow Fe\left(III\right)\)



 Mn ơi, giải hộ mik câu này với! Tối nay mik phải nộp rồi ạ! Cảm ơn mn nhiều lắm!
Mn ơi, giải hộ mik câu này với! Tối nay mik phải nộp rồi ạ! Cảm ơn mn nhiều lắm!


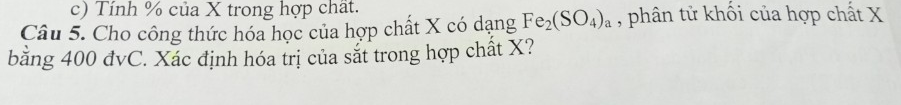
Câu 17:
a) PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
b+c) Ta có: \(n_{Mg}=\dfrac{3,6}{24}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,3\left(mol\right)\\n_{H_2}=0,15\left(mol\right)=n_{MgCl_2}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\\m_{ddHCl}=\dfrac{0,3\cdot36,5}{14,6\%}=75\left(g\right)\\m_{H_2}=0,15\cdot2=0,3\left(g\right)\\m_{MgCl_2}=0,15\cdot95=14,25\left(g\right)\end{matrix}\right.\)
d) Ta có: \(m_{dd}=m_{Mg}+m_{ddHCl}-m_{H_2}=78,3\left(g\right)\)
\(\Rightarrow C\%_{MgCl_2}=\dfrac{14,25}{78,3}\cdot100\%\approx18,2\%\)
a) $Mg + 2HCl \to MgCl_2 + H_2$
b) n H2 = n Mg = 3,6/24 = 0,15(mol)
V H2 = 0,15.22,4 = 3,36 lít
c) n HCl = 2n Mg = 0,3(mol)
=> m dd HCl = 0,3.36,5/14,6% = 75(gam)
d)
n MgCl2 = n Mg = 0,15(mol)
Sau phản ứng :
m dd = m Mg + mdd HCl - m H2 = 3,6 + 75 - 0,15.2 = 78,3(gam)
C% MgCl2 = 0,15.95/78,3 .100% = 18,2%