Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a.b.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,2 0,1 ( mol )
\(V_{O_2}=n_{O_2}.22,4=0,1.22,4=2,24l\)
c.\(3Fe+2O_2\rightarrow Fe_3O_4\)
0,1 0,05 ( mol )
\(m_{Fe_3O_4}=n_{Fe_3O_4}.M_{Fe_3O_4}=0,05.232=11,6g\)

a.b.\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{15,8}{158}=0,1mol\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,1 0,05 ( mol )
\(V_{O_2}=n_{O_2}.22,4=0,05.22,4=1,12l\)
c.\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,05 0,025 ( mol )
\(m_{Fe_3O_4}=n_{Fe_3O_4}.M_{Fe_3O_4}=0,025.232=5,8g\)

\(n_{KMnO4} = \dfrac{15,8}{158} = 0,1 (mol) \\ PTHH: 2KMnO_4 \rightarrow (t^o) K_2MnO_4 + MnO_2 + O_2 \\ Mol: 0,1 \rightarrow 0,05 \rightarrow 0,05 \rightarrow 0,05 \\ 3Fe + 2O_2 \rightarrow (t^o) Fe_3O_4 \\ Mol:0,075 \leftarrow0,05 \leftarrow 0,025 \\ m_{Fe_3O_4} = 232 . 0,025 = 5,8(g)\)

\(n_{KMnO_4}=\dfrac{31,6}{158}=0,2mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,2 0,1 0,1 0,1
a)\(V_{O_2}=0,1\cdot22,4=2,24l\)
b)\(m_{CRắn}=m_{K_2MnO_4}+m_{MnO_2}=0,1\cdot197+0,1\cdot87=28,4g\)
c)\(n_{CH_4}=\dfrac{11,2}{22,4}=0,5mol\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
0,5 0,1 0 0
0,05 0,1 0,05 0,1
0,45 0 0,05 0,1
\(V_{CO_2}=0,05\cdot22,4=1,12l\)
\(m_{H_2O}=0,1\cdot18=1,8g\)
PTHH: 2KMnO4--to-> K2MnO4+MnO2+O2
0,2----------------0,1---------0,1-----0,1
b, nKMnO4= \(\dfrac{31,6}{158}\)=0,2 mol
Theo pt: nO2=\(\dfrac{1}{2}\).0,2=0,1 mol
=> VO2= 0,1.22,4= 2,24 l
=>m cr=0,1.197+0,1.87=28,4g
CH4+2O2-to>CO2+2H2O
0,5-----0,25-----0,5
n CH4=\(\dfrac{11,2}{22,4}\)=0,5 mol
=>Oxi du
=>V CO2=0,25.22,4=5,6l
=>m H2O=0,5.18=9g

a)nO2=\(\dfrac{3.36}{22.4}\)=0,15(mol)
2KMnO4(to)→K2MnO4+MnO2+O2
Theo PT: nKMnO4=2nO2=0,3(mol)
→m=mKMnO4=0,3.158=47,4(g)
b)nH2=\(\dfrac{8.96}{22.4}\)=0,4(mol)
2H2+O2(to)→2H2O
Vì \(\dfrac{nH_2}{2}\)<nO2→O2nH2 dư
Theo PT: nH2O=nH2=0,4(mol)
→mH2O=0,4.18=7,2(g)

a)\(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(m\right)\)
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
tỉ lệ :2 1 1 1
số mol :0,2 0,1 0,1 0,1
\(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
b)\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(m\right)\)
\(PTHH:3Fe+2O_2\underrightarrow{ }Fe_3O_4\)
theo phương trình ta có tỉ lệ\(\dfrac{0,2}{3}>\dfrac{0,1}{2}\)=>Fe dư
\(PTHH:3Fe+2O_2\xrightarrow[]{}Fe_3O_4\)
tỉ lệ :3 2 1
số mol :0,15 0,1 0,05
\(m_{Fe_3O_4}=0,05.232=11,6\left(g\right)\)

\(1) n_{KMnO_4}= \dfrac{31,6}{158} = 0,2(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{O_2} = \dfrac{1}{2}n_{KMnO_4} = 0,1(mol)\\ V_{O_2} = 0,1.22,4 = 2,24(lít)\\ 2) CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ V_{CH_4} = \dfrac{1}{2}V_{O_2} = 1,12(lít)\\ 3)n_{CH_4} = \dfrac{1,12}{22,4} = 0,05(mol)\\ \text{Nhiệt lượng tỏa ra = } = 0,05.880 = 44(KJ)\)

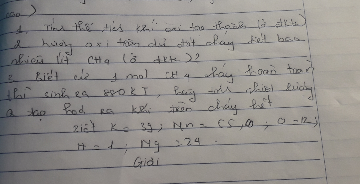
PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
a+b) Ta có: \(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\)
\(\Rightarrow n_{MnO_2}=n_{O_2}=0,1\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}m_{MnO_2}=0,1\cdot87=8,7\left(g\right)\\V_{O_2}=0,1\cdot22,4=2,24\left(l\right)\end{matrix}\right.\)
c) PTHH: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Theo PTHH: \(n_{Fe_3O_4}=\dfrac{1}{2}n_{O_2}=0,05\left(mol\right)\)
\(\Rightarrow m_{Fe_3O_4}=0,05\cdot232=11,6\left(g\right)\)