Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

![]()
= 12,8 + 2.0,3 = 13,4 g
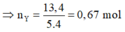
⇒ n H 2 p h ả n ứ n g = 0.
![]()
· Đốt cháy Y:
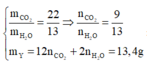
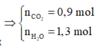
=> Đốt cháy X được:
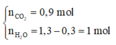
![]()
=> Đặt công thức chung cho X là C1,8H4.
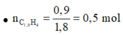
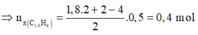
→
B
T
l
i
ê
n
k
ế
t
![]()
= 0,12 mol
![]()
=> Chọn đáp án A.

Đáp án C
Định hướng tư duy giải:
Ta có :

Trong Z có anken, ankan, và H2 dư :
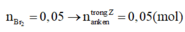

Trong Z
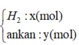
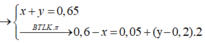
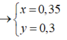
Số mol H2 phản ứng : 0,6-0,35=0,25(mol)
![]()
![]()

Đáp án A
Áp dụng định luật bảo toàn nguyên tố:
![]()
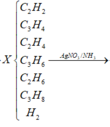
Khi cho T qua dung dịch nước brom thì C2H4, C2H4, C4H8, C4H6 phản ứng với brom.
![]() (1)
(1)
![]() (2)
(2)
Từ (1) và (2) có
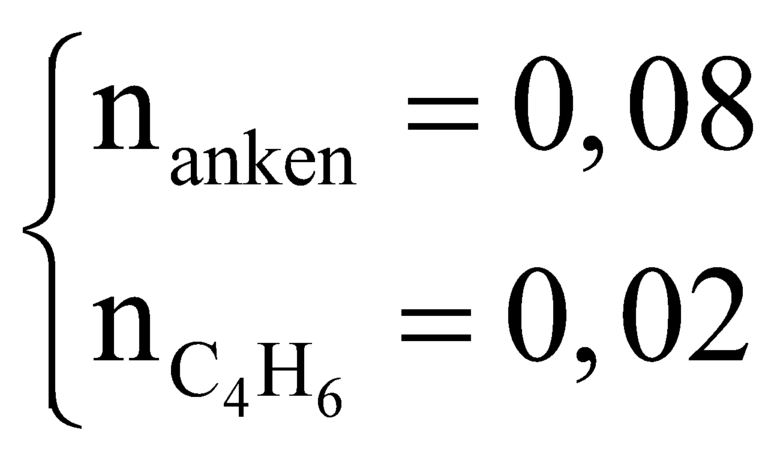
![]()

Đáp án A
Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni.
Nung bình → hhX có dX/H2 = 8.
Theo BTKL: mhhX = mhh ban đầu = 0,35 x 26 + 0,65 x 2 = 10,4 gam
→ nhhX = 10,4 : 16 = 0,65 mol.
→ nH2phản ứng = nhh ban đầu - nX = 0,35 + 0,65 - 0,65 = 0,35 mol.
Ta có: nπ trước phản ứng = 2 x nCH≡CH = 2 x 0,35 = 0,7 mol.
→ nπ dư = nπ trước phản ứng - nH2 = 0,7 - 0,35 = 0,35 mol.
• Ta có nπ dư = 2 x nAgC≡CAg + nBr2
→ nBr2 = 0,35 - 2 x (12 : 240) = 0,25 mol

Đáp án B
Tóm tắt quá trình:
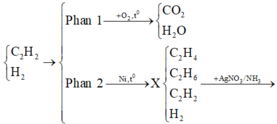
Ở mỗi phần gọi 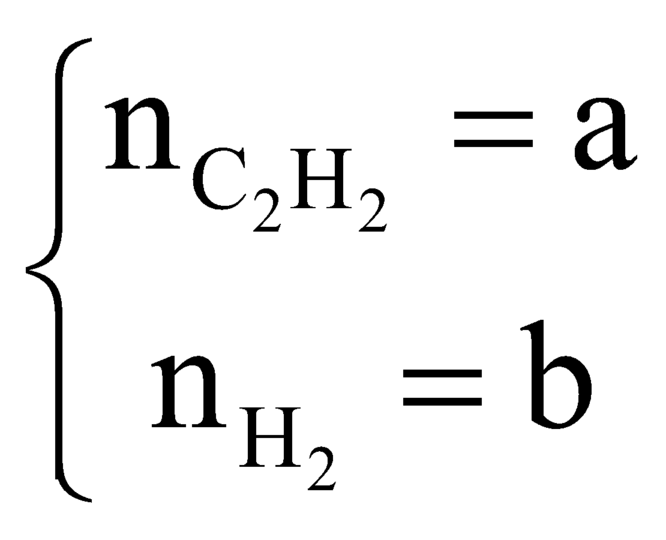
Khi đốt cháy hoàn toàn phần 1 thì
![]() (1)
(1)
Khi đốt cháy hoàn toàn Y thì
![]()
Mặt khác đốt cháy hoàn toàn hỗn hợp X cũng giống như đốt cháy hoàn toàn hỗn hợp ở phần 1
Nên ![]()
![]()
Mà ![]()
![]()
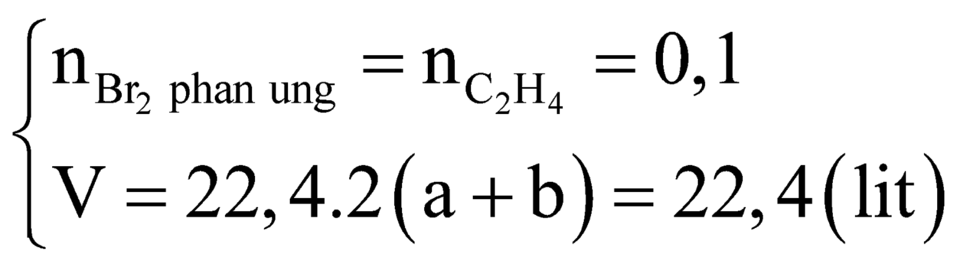
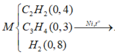
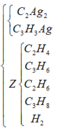
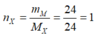
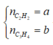
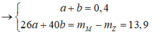
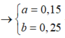
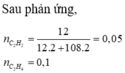
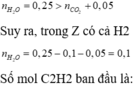
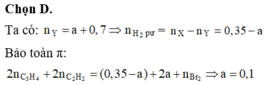
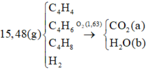
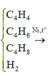
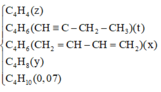
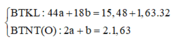
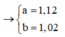
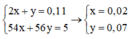
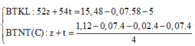
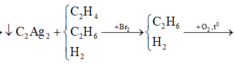
$C_2H_2+2H_2\xrightarrow{t^o,Ni}C_2H_6(1)$
$C_2H_2+2AgNO_3+2NH_3\to C_2Ag_2\downarrow+NH_4NO_3(2)$
$C_2H_2+2Br_2\to C_2H_2Br_4(3)$
$2C_2H_6+7O_2\xrightarrow{t^o}4CO_2+6H_2O$
Theo PT:
$n_{C_2H_2(2)}=n_{C_2Ag_2}=\frac{24}{240}=0,1(mol)$
$n_{C_2H_2(3)}=\frac{1}{2}n_{Br_2}=\frac{1}{2}.\frac{40}{160}=0,125(mol)$
$n_{C_2H_6}=\frac{1}{3}n_{H_2O}=\frac{1}{3}.\frac{11,7}{18}=\frac{13}{60}(mol)$
Sau pứ (1):
$n_{C_2H_2(dư)}=0,125+0,1=0,225(mol)$
Theo PT(1): $n_{C_2H_2(pứ)}=\frac{13}{60}(mol);n_{H_2}=\frac{13}{30}(mol)$
$\to a=n_{C_2H_2}+n_{H_2}=\frac{13}{60}+\frac{13}{30}+0,225=\frac{7}{8}(mol)$