Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phản ứng nhiệt nhôm:
![]()
X tác dụng với NaOH thu được => Al dư (*)
Phản ứng xảy ra hoàn toàn (**)
Kết hợp (*), (**) => F e 3 O 4 hết => X gồm Fe, A l 2 O 3 và Al dư
Chú ý: Bài toán chia làm hai phần không bằng nhau
*Xét phần một
Số mol H2 thu được là: ![]()
Trong X, chỉ có Al2O3 và Al dư tác dụng với NaOH theo sơ đồ sau:
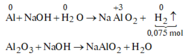
![]()
![]()
Chất rắn thu được là Fe
Chất rắn thu được tác dụng với H2SO4 đặc, nóng:
Sơ đồ phản ứng:
![]()
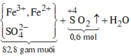
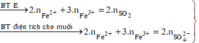
![]()
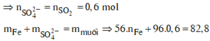
![]()
![]()
![]()
![]()
![]()
![]()
![]()
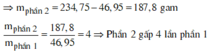
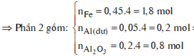
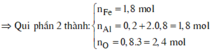
*Xét phần hai:
Số mol HNO3 là: ![]()
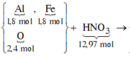
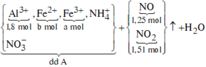
Các quá trình tham gia của H+:
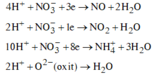
![]()
![]()
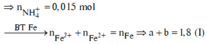
![]()
![]()
![]()


Đáp án A
Ta có khối lượng mỗi phần là 30,66 gam.
Cho phần một tác dụng với NaOH dư thu được 0,09 mol H2 do vậy trong X chứa Al dư.
Vậy trong mỗi phần chứa Fe, Al2O3 và Al dư 0,06 mol.
Cho phần 2 tác dụng với 1,74 mol HNO3 thu được 0,18 mol NO. Cô cạn dung dịch Y thu được các muối, nung rắn tới khối lượng không đổi thu được rắn chứa Al2O3 và Fe2O3 có số mol bằng nhau.
Gọi số mol của Fe, Al2O3 trong mỗi phần lần lượt là a, b
=> 56a+102b+0,06.27= 30,66
Và a= 2b+0,06
Giải hệ: a=0,3; b=0,12.
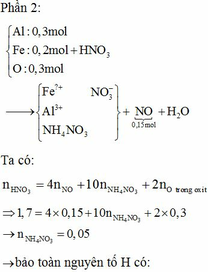
Gọi x là số mol NH4NO3 có thể tạo ra.
Bảo toàn N: n N O 3 - t r o n g m u o i K L = 1 , 74 - 0 , 18 - 2 x = 1 , 56 - 2 x
Bảo toàn e: 1,56-2x= 0,12.6+0,18.3+8x
Vậy NO3– trong muối là 1,5 mol.
Muối trong Y gồm Al(NO3)3 0,3 mol, Fe(NO3)2 0,3 mol và NH4NO3 0,03 mol.
Cho Y tác dụng với Na2CO3 dư thu được kết tủa là Al(OH)3 0,3 mol và FeCO3 0,3 mol.
=> a= 58,2 gam

Chọn đáp án A.
![]()
· Phần 1 + NaOH dư → 0,075 mol H2 + 5,6g Fe
n A l = 2 3 n H 2 = 0 , 05 m o l
n A l p h ả n ứ n g = n F e = 5 , 6 56 = 0 , 1 m o l
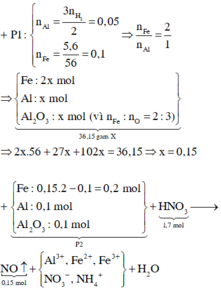
· Phần 2 + 1,7 mol HNO3 → 0,15 mol NO + m gam muối
=> HNO3 phản ứng hết.
Giả sử phần 2 có khối lượng gấp k lần phần 1.
![]()
⇒ k = 2
=> Phần 2 gồm: 0,2 mol Fe, 0,1 mol Al, 0,1 mol Al2O3.
Đặt a, b lần lượt là số mol của Fe2+, Fe3+ tạo thành.
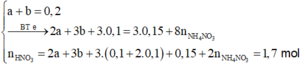
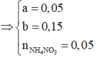
![]()
Gần nhất với giá trị 113


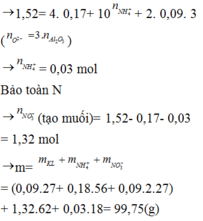




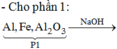
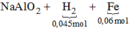
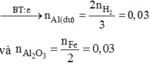
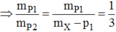
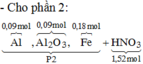
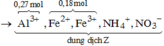

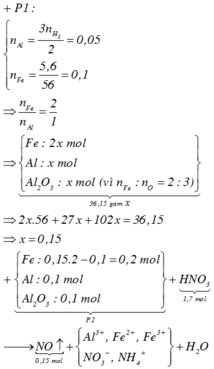
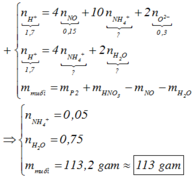

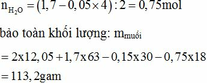

Đáp án A