Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

b1
cho m gam hỗn hợp gồm Zn và S vào bình không có không khí ,nung bình sau một thời gian thu được chất
b2
Fe+Sto→FeS
Ta có: nFe=5,6\56=0,1 mol; nS=3,2\32=0,1 moln
VÌ số mol hai chất bằng nhau theo đúng tỉ lệ phản ứng nên tính hiệu suất theo chất nào cũng được.
Gọi số mol Fe phản ứng là x
→nFeS=nFe phản ứng=x mol; nFe dư=0,1−x mol\
FeS+2HCl→FeCl2+H2S\
Fe+2HCl→FeCl2+H2\
→nH2S=nFeS=x mol; nH2=nFe dư=0,1−x mol\
→nY=x+0,1−x=0,1 mol; mY=34.x+2.(0,1−x)=0,1.10,6.2→x=0,06 mol
Hiệu suất phản ứng: H=0,06\0,1=60%

Đáp án A
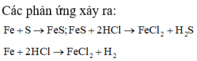
Hỗn hợp khí Z gồm H2S và H2. Đặt nFe=1mol . Dựa vào phương trình phản ứng ta thấy vì số mol khí sinh ra luôn là 1 mol với bất kì hiệu suất và tỉ lệ a:b nào nên:
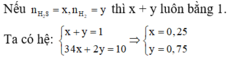
Theo đề bài hiệu suất phản ứng là 50% nhưng do chưa biết Fe hay S dư nên phải xét hai trường hợp. Tuy nhiên khi nhìn vào đáp án có thể thấy số mol sắt lớn hơn số mol lưu huỳnh nên hiệu suất được tính theo lưu huỳnh. Bảo toàn lưu huỳnh suy ra
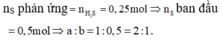

Đáp án A
Các phản ứng xảy ra:
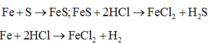
Hỗn hợp khí Z gồm H2S và H2. Đặt nFe=1mol . Dựa vào phương trình phản ứng ta thấy vì số mol khí sinh ra luôn là 1 mol với bất kì hiệu suất và tỉ lệ a:b nào nên:
Nếu ![]() thì x + y luôn bằng 1. Ta có hệ:
thì x + y luôn bằng 1. Ta có hệ:
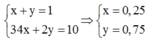
Theo đề bài hiệu suất phản ứng là 50% nhưng do chưa biết Fe hay S dư nên phải xét hai trường hợp. Tuy nhiên khi nhìn vào đáp án có thể thấy số mol sắt lớn hơn số mol lưu huỳnh nên hiệu suất được tính theo lưu huỳnh. Bảo toàn lưu huỳnh suy ra
nS phản ứng
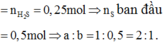

a) PTHH : Fe + S \(\rightarrow\) FeS
=> A gồm : Fe , FeS
Fe + 2 HCl -> FeCl2 + H2
FeS + 2 HCL -> FeCl2 + H2S
=> Y gồm : H2 , H2S
nY = n H2 + n H2S = 0,1 mol (I)
dY/H2 = 13 -> m Y = 2.nH2 + 34.n H2S = 13.2.0,1 = 2,6 g (II)
Từ (I),(II) => n H2 = 0,025 mol ; n H2S = 0,075 mol
Fe + 2 HCl \(\rightarrow\) FeCl2 + H2
0,025<---------------------0,025 mol
FeS + 2 HCl \(\rightarrow\) FeCl2 + H2S
0,075<-------------------------0,075 mol
Ta có: n S = n Fe phản ứng = n FeS = 0,075 mol
=>m S =0,075.32 = 2,4 g
n Fe ban đầu = 0,075 + 0,025 = 0,1mol
=>m Fe=0,1.56 = 5,6 g
=> %m S = \(\dfrac{2,4}{2,4+5,6}.100=30\%\)
=> %m Fe = 100 - 70 = 30%
b ) 2 H2 + O2 \(\rightarrow\) 2 H2O
0,025-------------->0,025 mol
2 H2S + 3 O2 \(\rightarrow\) 2 SO2 + 2 H2O
0,075--------------->0,075--->0,075 mol
m H2O2 = 5,1 g -> n H2O2 = 0,15 mol
PTHH : SO2 + H2O2 \(\rightarrow\) H2SO4
Ban đầu :0,075---->0,15 mol
Phản ứng:0,075--->0,075------>0,075 mol
Sau phản ứng:0----->0,075----->0,075 mol
m dd sau phản ứng = 18.(0,025 + 0,075 ) + 64.0,075 + 100 = 106,6 g
m H2O2 dư = 0,075.34 =2,55g
\(\Rightarrow C\%_{H_2O_2dư}=\dfrac{2,55}{106,6}.100=2,392\%\)
m H2SO4 = 0,075.98 = 7,35g
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{7,35}{106,6}.100=6,895\%\)

A + H2SO4 → Hỗn hợp khí ⇒ Fe dư; khí Y gồm: H2 ( x mol) và H2S (y mol)
⇒ x + y = 0,1 mol (1)
Bảo toàn S: nH2S = nFeS = nS = y mol
nFe dư = nH2 = x
Bảo toàn Fe: nFe = nFeS + nFe dư = x + y
mX = 56(x + y ) + 32y = 7,2g (2)
Từ (1)(2) ⇒ x = 0,05 mol; y = 0,05 mol
MY = mY : nY = (0,05.2 + 0,05.34) : 0,1 = 18 ⇒ dY/H2 = 9
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{FeS}=b\left(mol\right)\end{matrix}\right.\left(đk:a,b>0\right)\)
TH1: S dư
Vậy toàn bộ lượng khí sinh ra là H2S
\(d_{Y\text{/}H_2}=d_{H_2S\text{/}H_2}=\dfrac{34}{2}=17\)
TH2: Fe dư
\(n_{khí}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Bảo toàn KL: \(m_A=m_X=7,2\left(g\right)\)
PTHH:
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a----------------------------->a
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
b-------------------------------->b
Ta có hệ phương trình: \(\left\{{}\begin{matrix}56a+88b=7,2\\a+b=0,1\end{matrix}\right.\)
\(\Leftrightarrow a=b=0,05\left(TM\right)\)
\(M_Y=\dfrac{0,05.\left(2+34\right)}{0,1}=18\left(g\text{/}mol\right)\\ \rightarrow d_{Y\text{/}H_2}=\dfrac{18}{2}=9\)
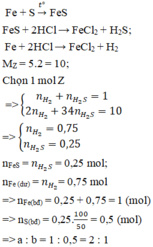
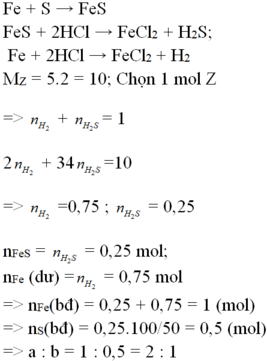


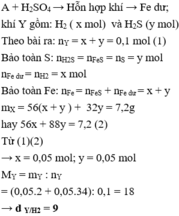
\(Fe+S\underrightarrow{^{to}}FeS\)
Ta có:
\(n_{Fe}=\frac{5,6}{56}=0,1\left(mol\right)\)
\(n_S=\frac{3,2}{32}=0,1\left(mol\right)\)
Vì số mol hai chất bằng nhau theo đúng tỉ lệ phản ứng nên tính hiệu suất theo chất nào cũng được.
Gọi số mol Fe phản ứng là x
\(\Rightarrow n_{FeS}=n_{Fe\left(pư\right)}=x\left(mol\right);n_{Fe\left(dư\right)}=0,1-x\left(mol\right)\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\Rightarrow n_{H2S}=n_{FeS}=x\left(mol\right),n_{H2}=n_{Fe\left(dư\right)}=0,1-x\left(mol\right)\)
\(\Rightarrow n_Y=x+0,1-x=0,1\left(mol\right)\)
\(\Rightarrow m_Y=34.x+2\left(0,1-x\right)=0,1.10,6.2\)
\(\Rightarrow x=0,06\left(mol\right)\)
\(\Rightarrow H=\frac{0,06}{0,1}=60\%\)
bạn bấm vào trang cá nhân của mình thì sẽ thấyNguyễn Hoàng Yến Nhi