Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
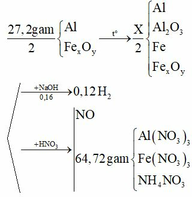
nNaOH = nNaAlO2 = nAl + 2nAl2O3 trong 0,5X = 0,16 = nAl ban đầu
nAl trong 0,5X = 0,12/1,5 = 0,08 Þ nAl2O3 = (0,16 - 0,08)/2 = 0,04
Þ nO ban đầu = 0,04x3x100/75 = 0,16
Þ mFe ban đầu = 27,2/2 - 0,16x16 - 0,16x27 = 6,72 Þ nFe ban đầu = 6,72/56 = 0,12
Þ x/y = 0,12/0,16 = 3/4 Þ Fe3O4
mMuối = 0,16x213 + 0,12x242 + 80xnNH4NO3 = 64,72 Þ nNH4NO3 = 0,02
BTE Þ 0,16x3 + 0,12 = 3nNO + 8x0,02 Þ nNO = 0,12 Þ V = 0,12x22,4 = 2,688

Khối lượng từng phần là : ![]()
Phản ứng nhiệt nhôm: 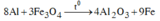
=> Hỗn hợp X gồm Al2O3, Fe, Al dư, Fe3O4 dư
Xét phần hai:
X tác dụng với dung dịch HNO3 cũng chính là hỗn hợp ban đầu Al (a mol) và Fe3O4 (b mol) tác dụng với dung dịch HNO3
![]()
Quy đổi hỗn hợp ban đầu thành Al: a mol; Fe: 3b mol; O:4b mol
Sơ đồ phản ứng:
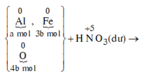
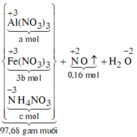
![]()
![]()
![]()
![]()
![]() ]
]
![]()
![]() c = 0,0375 mol
c = 0,0375 mol
-Xét phần một:
Số mol H2 thu được là: ![]()
Sơ đồ phản ứng tạo khí H2 : 
![]()
![]()
![]()
![]()
-Xét phản ứng nhiệt nhôm:
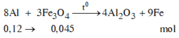
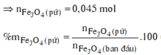
![]()
Đáp án B.

Đáp án B
Quy đổi phần 1: thành 3 nguyên tố Al, Fe, O với số mol tương ứng là x, y, z.
27x + 56y + 16z = 14,49. (1)
Khi tác dụng với HNO3 dư thu khí NO: 0,165 mol.
Bảo toàn electron: 3x + 3y – 2z = 3nNO
3x + 3y – 2z = 3.0,165 = 0,495 (2)
Quy đổi phần 2: Al, Fe, O với số mol tương ứng là:kx, ky, kz
( Vì đề bài cho hai phần không bằng nhau)
Khi tác dụng với NaOH . Fe không phản ứng.
Bte: 3nAl – 2nO = 2nH2
3kx – 2kz = 0,03 (3)
Rắn còn lại là Fe: ky = 0,045 (4).
Lấy (3)/(4) → 3 x - 2 z y = 2 3 → 9x -2y – 6z – 0(4)
→ x = 0,15, y = 0,135, z = 0,18
Công thức oxit: y 2 = 0 , 135 0 , 18 = 3 4 → F e 3 O 4
(4) → k = 0 , 045 0 , 135 = 1 3
m d a u = m 1 + m 2 = m 1 + m 1 3 = 4 m 1 3 = 27 . 0 , 15 + 56 . 0 , 135 + 16 . 0 , 18 . 4 3 = 19 , 32 g
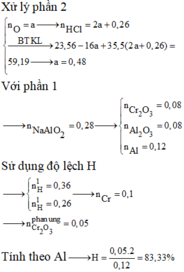




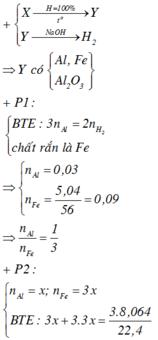
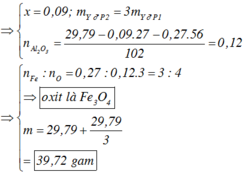

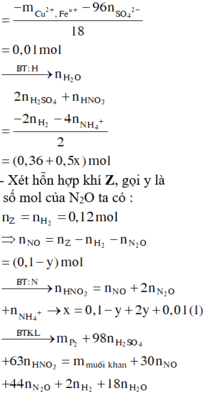




Chọn đáp án C
nNaOH phản ứng = nNaAlO3 sau phản ứng = 0,16
nAl trong 0,5X = 0,12/1,5 = 0,08 mol =>phản ứng
BTE => a - (0,08.3 + 0,09.3 + 0,01 - 0,02.8)/3 = 0,12