

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án : A
Khi đường thẳng nàm ngang thì lúc này kết tủa ổn địch chỉ còn duy nhất BaSO4
=> nBaSO4 = nSO4 = 0,3x = 0,03 mol => x = 0,1M
Nếu nBa(OH)2 = 0,02 ; nNaOH = 0,03 mol
=> nOH = 0,07 ; nAl3+ = 0,02
=> nAl(OH)3 = 4nAl3+ - nOH = 0,01 mol và nBaSO4 = nBa2+ = 0,02 mol
=> mkết tủa = 5,44g

Đáp án A.
Theo đồ thị n S O 4 2 - = 0,03 mol → n A l 2 ( S O 4 ) 3 = 0,01 mol
Hỗn hợp bazơ gồm: Ba2+ (0,02 mol); Na+ (0,03 mol) và OH- (0,7 mol) tác dụng với dung dịch A gồm: Al3+ (0,02 mol) và SO42- (0,03 mol) ta có PTHH:
Ba2+ + SO42- → BaSO4
0,02---------------0,02 mol
Al3+ + 3OH- → Al(OH)3
0,02---0,06------0,02 mol
Al(OH)3 + OH- → AlO2- + 2H2O
0,01---------0,01
Khối lượng kết tủa = m B a S O 4 + m A l ( O H ) 3 = 5,44 gam

Đáp án B
Dựa vào đồ thị thấy tại 6,99 gam thì lượng kết tủa không đổi → tại đó chỉ có kết tủa BaSO4: 0,03 mol → a = (0,03 : 3): 0,1 = 0,1
Nếu cho (Ba(OH)2 0,02 mol và NaOH 0,03 mol) + Al2(SO4)3: 0,01mol
Thấy 3< n O H - : n A l 3 + < 4 → Tạo đồng thời Al(OH)3: x mol và AlO2-: y mol
Ta có hệ phương trình
x + y = 0 , 02 3 x + 4 y = 0 , 07 → x = 0,01; y = 0,01
Mặt khác: n S O 4 2 - = 0,03 mol > n B a 2 + = 0,02 mol → BaSO4 ; 0,02 mol
→ m k t = m A l ( O H ) 3 + m B a S O 4 = 0,01*78 + 0,02*233 = 5,44 gam

Chọn đáp án B
Nhìn đồ thị ta thấy có 3 giai đoạn
+ giai đoạn 1: đồ thị đi lên khi xảy ra phản ứng:
3Ba(OH)2 + Al2(SO4)3→ 3BaSO4↓ + 2Al(OH)3↓ (1)
+ giai đoạn đồ thị đi xuống là do Ba(OH)2 đang hòa tan kết tủa Al(OH)3↓ theo phản ứng
Ba(OH)2 + 2Al(OH)3→ Ba(AlO2)2 + 4H2O (2)
+ giai đoạn đồ thị đi ngang khi phản ứng (2) Al(OH)3 bị hòa tan hoàn toàn, chỉ còn lại kết tủa BaSO4
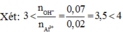
nBa(OH)2 = 0,1. 0,2 = 0,02 (mol) ; nNaOH = 0,1.0,3 = 0,03 (mol) ; nAl2(SO4)3 = 0,1.0,1 = 0,01 (mol)
=> ∑ nOH- = 2nBa(OH)2 + nNaOH = 2. 0,02 + 0,03 = 0,07 (mol)
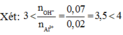
Có các phản ứng xảy ra:
Ba2+ + SO42-→ BaSO4↓
0,02 → 0,02 (mol)
3OH- + Al3+ → Al(OH)3↓
4OH- + Al3+ → AlO2− + H2O
Áp dụng công thức nhanh:
nOH- = 4nAl3+ - nAl(OH)3
=> nAl(OH)3 = 4nAl3+ - nOH- = 4.0,02 – 0,07 = 0,01 (mol)
=> m↓ = mAl(OH)3 + mBaSO4 = 0,01.78 + 0,02.233 = 5,44 (g) gần nhất với 5,45 (g)

Chọn B.
- Các phương trình phản ứng:
B a 2 + + S O 4 2 - → B a S O 4 ( k t )
3 O H - + A l 3 + → A l ( O H ) 3
A l ( O H ) 3 + O H - → A l O 2 - + H 2 O (tan vào dung dịch)
- Trên đồ thị, ta thấy: n B a S O 4 = m B a S O 4 233 = 2 , 796 233 = 0 , 012 m o l
- Để lượng kết tủa không đổi thì: n O H - m i n = 4 n A l 3 +
Với: n A l 3 + = 2 / 3 n S O 4 2 - = 2 / 3 . 0 , 012 = 0 , 008 m o l ⇒ n O H - m i n = 4 . 0 , 008 = 0 , 032 m o l
- Thể tích dung dịch Ba(OH)2 nhỏ nhất cần dùng là:
V B a ( O H ) 2 = 0 , 032 2 . 0 , 2 = 0 , 08 lít = 80 ml.