Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
Tại V thì kết tủa chỉ chứa BaSO4 với
n B a S O 4 = 69 , 9 233 = 0 , 3 m o l → n A l 2 ( S O 4 ) 3 = n B a S O 4 3 = 0 , 1 m o l ⇒ n B a ( O H ) 2 = 4 n A l 3 + 2 = 8 n A l 2 ( S O 4 ) 3 2 = 0 , 4 m o l ⇒ V B a ( O H ) 2 = 2 l í t

Chọn B.
Các phương trình phản ứng có thể xảy ra là:
B a 2 + + S O 4 2 - → B a S O 4 ( k t ) A l 3 + + O H - → A l ( O H ) 3 A l ( O H ) 3 + O H - → A l ( O H ) 4 -
Tại vị trí thể tích dung dịch Ba(OH)2 thì có kết tủa BaSO4 và dung dịch A l ( O H ) 4 -
n k t = 0 , 3 m o l ⇒ n S O 4 2 - = n k t = 0 , 3 m o l ⇒ n A l 3 + = 0 , 2 m o l ⇒ n O H - = 4 n A l 3 + = 0 , 8 m o l ⇒ n B a ( O H ) 2 = 1 / 2 . n O H - = 0 , 4 m o l ⇒ V = 0 , 4 0 , 2 = 2 l í t

Chọn B
mBaSO4 = 69,9 ⇒ nBaSO4 = 0,3 ⇒ nAl2(SO4)3 = 0,1 ⇒ nAl3+ = 0,2
Tại giá trị V, kết tủa Al(OH)3 đã tan hết ⇒ nOH- = 4nAl3+ = 0,8 ⇒ nBa(OH)2 = 0,4 ⇒ V = 2

Chọn B
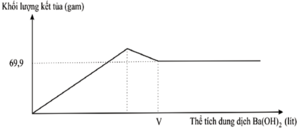
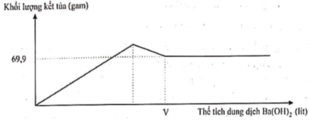
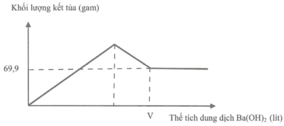
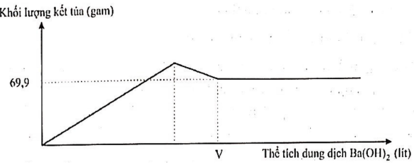
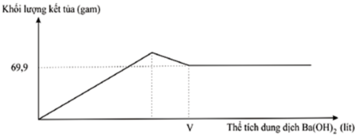
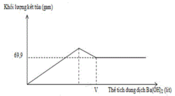
Giải thích các quá trình biến thiên trong đồ thị:
Đoạn 1: Đi lên, do sự tạo thành BaSO4 và Al(OH)3
Đoạn 2: Đi xuống, do sự hòa tan kết tủa Al(OH)3
Đoạn 3: Đi ngang, do BaSO4 không tan.
Từ đồ thị ta thấy giá trị m = 69,9 gam không đổi khi thể tích Ba(OH)2 thay đổi
=> m↓ = mBaSO4 = 69,9 (gam) => nBaSO4 = 69,9 : 233 = 0,3 (mol)
nAl2(SO4)3 = 1/3 nBaSO4 = 0,1 (mol) => nAl3+ = 2nAl2(SO4)3 = 2. 0,1 = 0,2 (mol)
Theo công thức tính nhanh, xuất hiện kết tủa, sau đó kết tủa tan: nOH- = 4nAl3+ - n↓
=> 0,4V = 4.0,2 – 0
=> V = 2 (lít)
Gần nhất với 2,1 lít






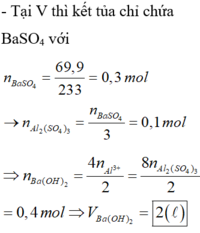
Đáp án B