Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
● Ta có: nBa2+ = 0,3 mol và ∑nSO42– = 0,35 mol.
⇒ nBaSO4 = 0,3 mol ⇒ mBaSO4 = 0,3 × 233 = 69,9 gam.
● Ta có ∑nOH– = 0,8 mol. và nZn2+ = 0,25 mol.
⇒ nZn(OH)2 = 4nZn2+ – ∑nOH– = 0,2 mol.
⇒ mZn(OH)2 = 0,2 × 99 = 19,8 gam.
⇒ Tổng khối lượng kết tủa = 69,9 + 19,8 = 89,7 gam ⇒ Chọn B
nZn(OH)2 = 4nZn2+ – ∑nOH– = 0,2 mol Bn giải thích hộ mình vs mình o hiểu lắm

Chọn D.
Ta có:
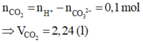
Dung dịch E có chứa SO42- (0,2 mol) và ![]()
Kết tủa gồm BaSO4 (0,2 mol) và BaCO3 (0,3 mol) Þ m = 105,7 (g)

Đáp án A
Gọi nNa = nBa = x (mol)
nH2SO4 = 0,125 (mol); nCuSO4 = 0,125 (mol) ; nH2 = 0,15 (mol)
Ta thấy: nH2 = 0,15 (mol) > nH2SO4 => Na, Ba phản ứng hết với axit sau đó tiếp tục phản ứng với H2O
Ta có: ∑ ne (KL nhường) = ∑ n e( H2 nhận)
=> x + 2x = 0,15.2
=> x = 0,1 (mol)
=> nOH- = 2 ( nH2 – nH2SO4) = 2 ( 0,15 – 0,125) = 0,05 (mol)
=> nCu(OH)2 = ½ nOH- = 0,025 (mol)
m↓ = mCu(OH)2 + mBaSO4 = 0,025.98 + 0,1.233 = 25,75 (g)
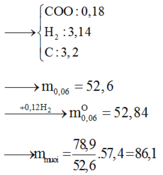







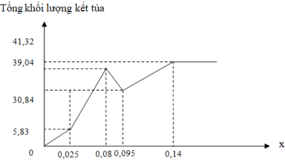
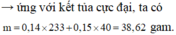
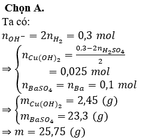
Chọn B
Vì: nBa = nBa(OH)2 = 0,3 mol
nSO4 = nH2SO4 + nZnSO4 = 0,325 mol
nOH = 0,8 mol ; nH+ = 0,25 mol ; nZn2+ = 0,2 mol
Ba2+ + SO42- → BaSO4
0,3 → 0,3 mol
nOH (pứ Zn2+) = 0,8 – nH+ = 0,55 mol
=> nOH : nZn2+ = 2,75 => Kết tủa hòa tan 1 phần
=> nZn(OH)2 = 2 nZn2+ – 0,5 nOH = 0,125 mol
=> m = 82,275g