Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


a. Các phương trình có thể xảy ra:
C + O2 → t ∘ CO2 (1)
CaCO3 → t ∘ CaO + CO2 (2)
MgCO3 → t ∘ MgO + CO2 (3)
CuCO3 → t ∘ CuO + CO2 (4)
C +CO2 → t ∘ 2CO (5)
C + 2CuO → t ∘ 2Cu + CO2 (6)
CO + CuO → t ∘ Cu + CO2 (7)
CaO + 2HCl →CaCl2 + H2O (8)
MgO + 2HCl →MgCl2 + H2O (9)
CuO + 2HCl →CuCl2 + H2O (10)
b. Vì sau phản ứng có CO và CO2, các phản ứng xảy ra hoàn toàn nên các chất còn lại sau khi nung là CaO, MgO và Cu không có phản ứng (10)
mCu = 3,2(g) => mCuCO3 = 6,2g
Gọi số mol CaCO3, MgCO3, C trong hỗn hợp lần lượt là a, b, c.(*)
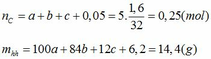
Giải ( *), (**), (***) ta được a=0,025; b=0,05; c=0,125.
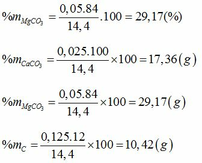

a, 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
x…………3/2.x
Fe + CuSO4 → FeSO4 + Cu
y……..y
Al phản ứng hết với CuSO4 sau đó Fe mới phản ứng với CuSO4. Vì sau phản ứng thu được rắn Y gồm 2 kim loại nên Al đã tan hết và Fe có thể đã phản ứng 1 phần hoặc chưa phản ứng. 2 kim loại trong Y là Fe và Cu.
⇒ nCu = nCuSO4 = 0,2.1 = 0,2 mol
⇒ mFe dư = mY - mCu = 15,68 - 0,2.64 = 2,88g
Đặt số mol Al ban đầu là x, số mol Fe phản ứng là y, ta có hệ phương trình:
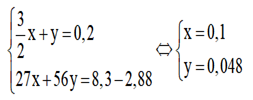
⇒ mAl = 0,1.27 = 2,7g
⇒ %mAl = 2,7/8,3.100 = 32,53%

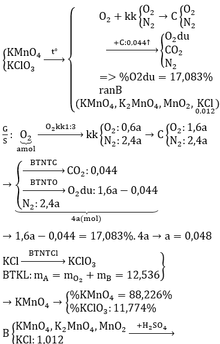

Gọi nKNO3 = a (mol); nKClO3 = b (mol)
\(\rightarrow\) 101a + 122,5b = 37,35 (1)
2KNO3 --- to --> 2KNO2 + O2
2KClO3 ---to --> 2KCl + 3O2
\(\rightarrow\) 85a + 74,5 b = 27,43 (2)
Giải hệ (1)(2) \(\Rightarrow\)a = 0,2 ; b = 0,14
%nKNO3 = 0,2 / (0,2 + 1,4) = 58,82%
%nKClO3 = 100% - 58,82% = 41,18%
Tương tự tính %m
Bảo toàn khối lượng:
mA = mB + mO2
\(\Leftrightarrow\)37,35 = 27,43 + mO2
\(\Leftrightarrow\) mO2 = 9,92 (g)
\(\Rightarrow\) nO2 = 9,92 / 32 = 0,31 (mol)
VO2 (đktc) = 0,31 . 22,4 = 6,944 (l)
VO2 (thường) = 0,31 . 24 = 7,44 (l)
AgNO3 + KCl -> AgCl + KNO3
0,14 ______ 0,14 ___ 0,14 _0,14 (mol)
Hiện tượng: Xuất hiện kết tủa trắng
mdd AgNO3 = (0,14 . 170)/17% = 140 (g)
\(\rightarrow\) mdd AgNO3 ban đầu = 140 + 10%.140 = 154 (g)
Bảo toàn khối lượng :
m dd sau pứ = mdd AgNO3 + mB - mAgCl
= 154 + 27,43 - 0,14.143,5
= 161,34 (g)
Dd sau pứ gồm: 0,14 mol KNO3, 14(g) AgNO3
C% KNO3 = (0,14 . 101)/161,34 .100%= 8,76%
C% AgNO3 = 14/161,34 . 100% = 8,68%
Mình không gõ được phân số, gõ mà nó không lên. Chả hiểu sao
Bạn thông cảm nha ^^