Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)\(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(m\right)\)
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
tỉ lệ :2 1 1 1
số mol :0,2 0,1 0,1 0,1
\(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
b)\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(m\right)\)
\(PTHH:3Fe+2O_2\underrightarrow{ }Fe_3O_4\)
theo phương trình ta có tỉ lệ\(\dfrac{0,2}{3}>\dfrac{0,1}{2}\)=>Fe dư
\(PTHH:3Fe+2O_2\xrightarrow[]{}Fe_3O_4\)
tỉ lệ :3 2 1
số mol :0,15 0,1 0,05
\(m_{Fe_3O_4}=0,05.232=11,6\left(g\right)\)

a)
\(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ \(\dfrac{0,3}{1}>\dfrac{0,25}{1}\)=> Hiệu suất tính theo H2
Gọi số mol CuO phản ứng là a
=> nCu = a (mol)
Có: (0,3-a).80 + 64a = 20,8
=> a = 0,2 (mol)
\(n_{H_2}=n_{CuO}=0,2\left(mol\right)\)
=> \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b) \(H\%=\dfrac{0,2}{0,25}.100\%=80\%\)

a) \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,4---------------------->0,6
=> V = 0,6.22,4 = 13,44 (l)
b)
\(n_{Fe_3O_4}=\dfrac{29}{232}=0,125\left(mol\right)\)
Gọi số mol Fe3O4 pư là a (mol)
PTHH: Fe3O4 + 4H2 --to--> 3Fe + 4H2O
Xét tỉ lệ: \(\dfrac{0,125}{1}< \dfrac{0,6}{4}\) => Hiệu suất tính theo Fe3O4
PTHH: Fe3O4 + 4H2 --to--> 3Fe + 4H2O
a----------------->3a
=> 232(0,125-a) + 56.3a = 22,6
=> a = 0,1
=> \(H\%=\dfrac{0,1}{0,125}.100\%=80\%\)
nAl = 10,8 : 27 = 0,4 (mol)
pthh : Al + 6HCl-t--> AlCl3 + H2
0,4--->2,4 (mol)
=> V= VO2 = 2,4 . 22,4 = 53,76 ( l)
nFe3O4 = 29 : 232 = 0,125 (mol)
pthh Fe3O4 + 4H2 -t--> 3Fe+ 4H2O
0,125----------------->0,375 (mol)
nFe (tt ) = 22,6 : 56 = 0,403 (mol )
%H = 0,375 / 0,403 . 100 % = 93 %

a, nFe = 16,8/56 = 0,3 (mol)
PTHH: Fe + 2HCl -> FeCl2 + H2
Mol: 0,3 ---> 0,6 ---> 0,3 ---> 0,3
VH2 = 0,3 . 22,4 = 6,72 (l)
b, nCuO = 20/80 = 0,25 (mol)
PTHH: CuO + H2 -> (t°) Cu + H2O
LTL: 0,25 < 0,3 => H2 dư
Gọi nCuO (p/ư) = a (mol)
=> nCu (sinh ra) = a (mol)
Ta có: 80(0,25 - a) + 64a = 16,4
=> a = 0,225 (mol)
H = 0,225/0,25 = 90%

nFe = 11.2/56=0.2 (mol)
3Fe + 2O2 -to-> Fe3O4
0.2____2/15____1/15
VO2 = 2/15 * 22.4 = 2.9867 (l)
mFe3O4 = 1/15 * 232 = 15.47 (g)
ta có pthh: 3Fe + 2O2 → Fe3O4
Ta có nFe=\(\dfrac{m}{M}\)=\(\dfrac{11,2}{56}\)=0,2(mol)
nO2=2nFe=2*\(\dfrac{0,2}{3}\)=\(\dfrac{2}{15}\)(mol)
VO2=n*M=16*\(\dfrac{2}{15}\)=2,13(l)
nFe3O4=\(\dfrac{0,2}{2}\)=0,1(mol)
mFe3O4=\(\dfrac{0,1}{168+64}\)=23,2(g)

$2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2$
$a\bigg)$
$n_{KMnO_4}=\frac{15,8}{158}=0,1(mol)$
Chất rắn sau p/ứ là $K_2MnO_4,MnO_2$
Theo PT: $n_{K_2MnO_4}=n_{MnO_2}=0,05(mol)$
$\to m_{\rm chất\, rắn}=0,05.197+0,05.87=14,2(g)$
$b\bigg)$
Vì $H=80\%\to n_{KMnO_4(p/ứ)}=0,1.80\%=0,08(mol)$
$\to n_{KMnO_4(dư)}=0,02(mol)$
Chất rắn sau p/ứ là $KMnO_4(dư):0,02;K_2MnO_4:0,04;MnO_2:0,04$
$\to m_{\rm chất\, rắn}=0,02.158+0,04.197+0,04.87=14,52(g)$
$c\bigg)$
Bảo toàn KL có:
$m_{O_2}=m_{KMnO_4}-m_{CR}$
$\to m_{O_2}=15,8-14,68=1,12(g)\to n_{O_2}=0,035(mol)$
Theo PT: $n_{KMnO_4(p/ứ)}=2n_{O_2}=0,07(mol)$
$\to H=\dfrac{0,07}{0,1}.100\%=70\%$

a.KClO3to⟶KCl+1,5O2
BTKL⟶mKClO3=mO2+mA
=>24,5=mO2+17,3
→O2→KClO3→H=75%
b.
4P + 5O2 → 2P2O5
0,16→ 0,2
Dư: 0,025
Sau pứ m(bình 1) = mP2O5 = 11,36 (g)
O2 + 2C → 2CO
0,025→ 0,05 0,05
Dư: 0,25
Sau pứ m(bình 2) = mCdư = 3 (g)

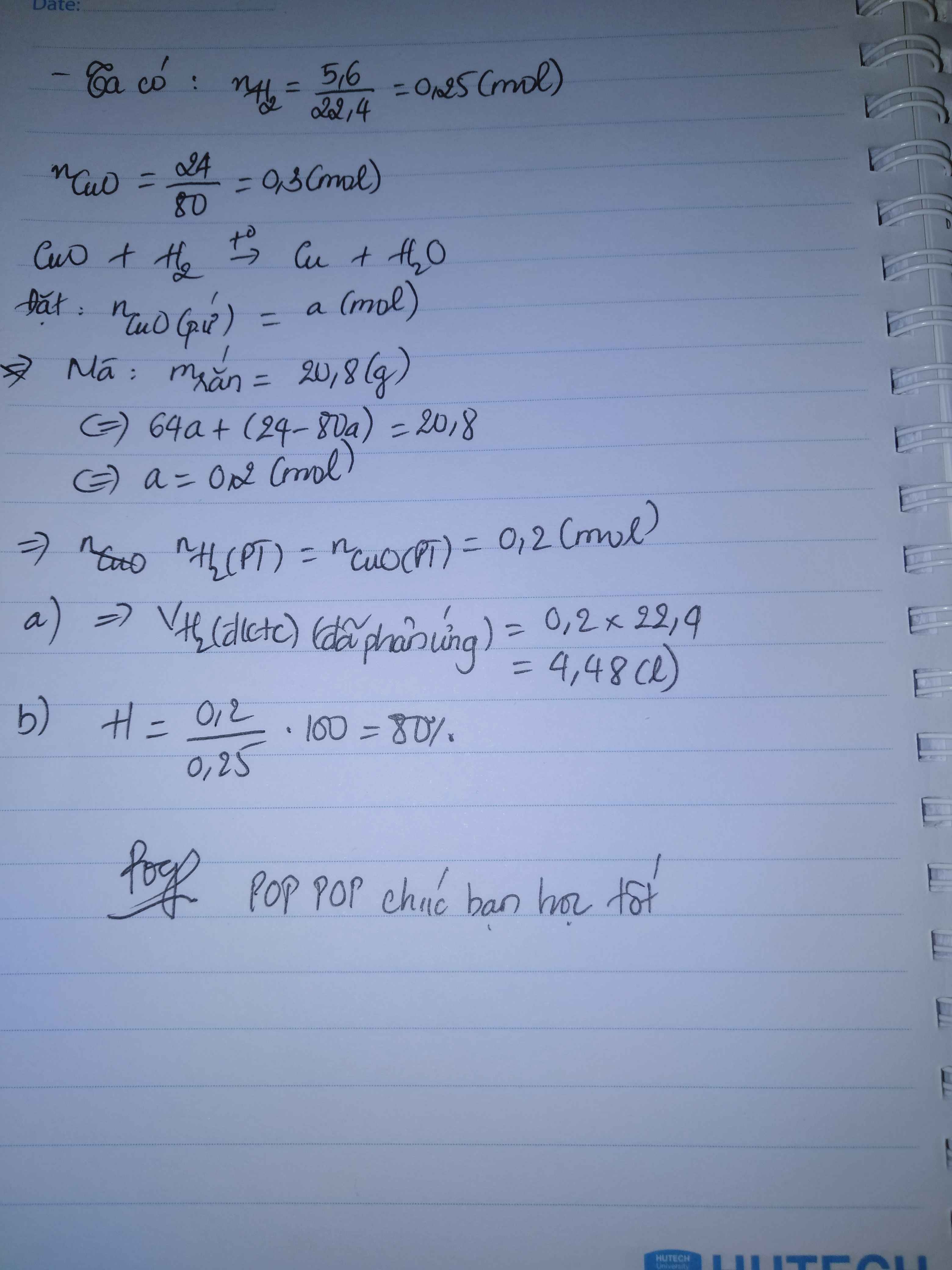
2KMnO4 (63/316 mol) \(\underrightarrow{t^o}\) K2MnO4 + MnO2\(\downarrow\) + O2\(\uparrow\) (63/632 mol).
a. Thể tích khí oxi thu được ở đktc là:
V=63/632.22,4=882/395 (lít).
b. Số mol khí oxi phản ứng là (14,4-11,2)/32=0,1 (mol) > 63/632 (mol).
Kết luận: Giả thiết câu b không xảy ra.