Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học:
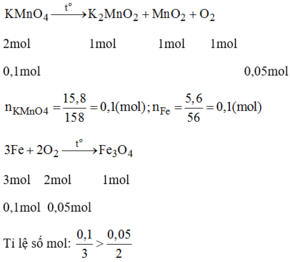
Vậy sắt còn dư nên khi đưa nam châm lại gần sản phẩm sau phản ứng thì nam châm bị hút.

2KMnO4 \(\xrightarrow[]{t^o}\) K2MnO4 + MnO2 + O2(1)
3Fe + 2O2 \(\xrightarrow[]{t^o}\) Fe3O4(2)
nKMnO4 = 15,8 : 158 = 0,1 mol
nFe = 5,6 : 56 = 0,1 mol
Theo pt 1 nO2 = \(\dfrac{1}{2}nKMnO_4=0,05mol\)
Lập tỉ lệ phương trình (2)
nFe : nO2 = \(\dfrac{0,1}{3}:\dfrac{0,05}{2}\)
Do 0,1/3 > 0,05/2 => Fe dư
Vậy sản phẩm thu được có Fe dư => bị nam châm hút

2KMnO4→→K2MnO4+MnO2+O2
\(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=\dfrac{1}{2}.\dfrac{15,8}{158}=0,05mol\\ n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ 3Fe+2O_2\rightarrow Fe_3O_4\\ \dfrac{0,1}{3}\approx0,33>\dfrac{0,05}{2}=0,25\)
Suy ra Fe dư=0,1-0,05.3:2=0,025 mol. Vậy sản phẩm gồm Fe3O4 và Fe dư nên nam châm vẫn hút.
\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: \(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\uparrow\left(1\right)\)
Theo PTHH(1): \(n_{O_2}=\dfrac{0,1.1}{2}=0,05\left(mol\right)\)
PTHH (2): \(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\left(2\right)\)
\(\left\{{}\begin{matrix}\dfrac{n_{Fe}}{3}=\dfrac{0,1}{3}=0,03\\\dfrac{n_{O_2}}{2}=\dfrac{0,05}{2}=0,025\end{matrix}\right.\) \(\Rightarrow\) Fe dư. O2 phản ứng hết
Vậy Fe còn dư nên sản phẩm sau ohanr ứng bị nam châm hút.

nAl=\(\dfrac{5,4}{27}\)=0,2mol
nO2=\(\dfrac{4,48}{22,4}\)=0,2mol
PTHH:
4Al + 3O2--to->2Al2O3
Tỉ lệ \(\dfrac{0,2}{4}\) <\(\dfrac{0,2}{3}\)->Al hết O2 dưtính theo Al
=>m O2=\(\dfrac{1}{60}\).32=\(\dfrac{8}{15}\)g
2KMnO4-to>K2MnO4+MnO2+O2
0,4--------------------------------------0,2
m KMnO4=0,4.158=63,2g
.

PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
a. Theo PTHH: \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=\dfrac{1}{2}0,1=0,05\left(mol\right)\)
\(\Rightarrow V_{O_2}=n_{O_2}.22,4=0,05.22,4=1,12\left(l\right)\)
b. PTHH: \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Ta có: \(\dfrac{1}{n_{O_2}}=\dfrac{1}{0,05}\)
\(\dfrac{1}{n_{Fe}}=\dfrac{1}{0,1}\)
\(\Rightarrow\dfrac{1}{n_{O_2}}>\dfrac{1}{n_{Fe}}\)
Vậy Fe dư
Theo PTHH: \(n_{Fe_3O_4}=\dfrac{0,1.1}{3}=\dfrac{1}{30}\left(mol\right)\)
\(\Rightarrow m_{Fe_3O_4}=n_{Fe_3O_4}.M_{Fe_3O_4}=\dfrac{1}{30}.232\approx7,73g\)

a.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(PTHH:2KMnO_4\underrightarrow{np}K_2MnO_4+MnO_2+O_2\)
2 1 1 1 ( mol )
0,2 0,1
\(V_{O_2}=n.22,4=0,1.22,4=2,24l\)
b.\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
3 2 1 ( mol )
0,2 0,1
0,1 0,1 0,05 ( mol )
\(m_{Fe_3O_4}=n.M=0,05.232=11,6g\)
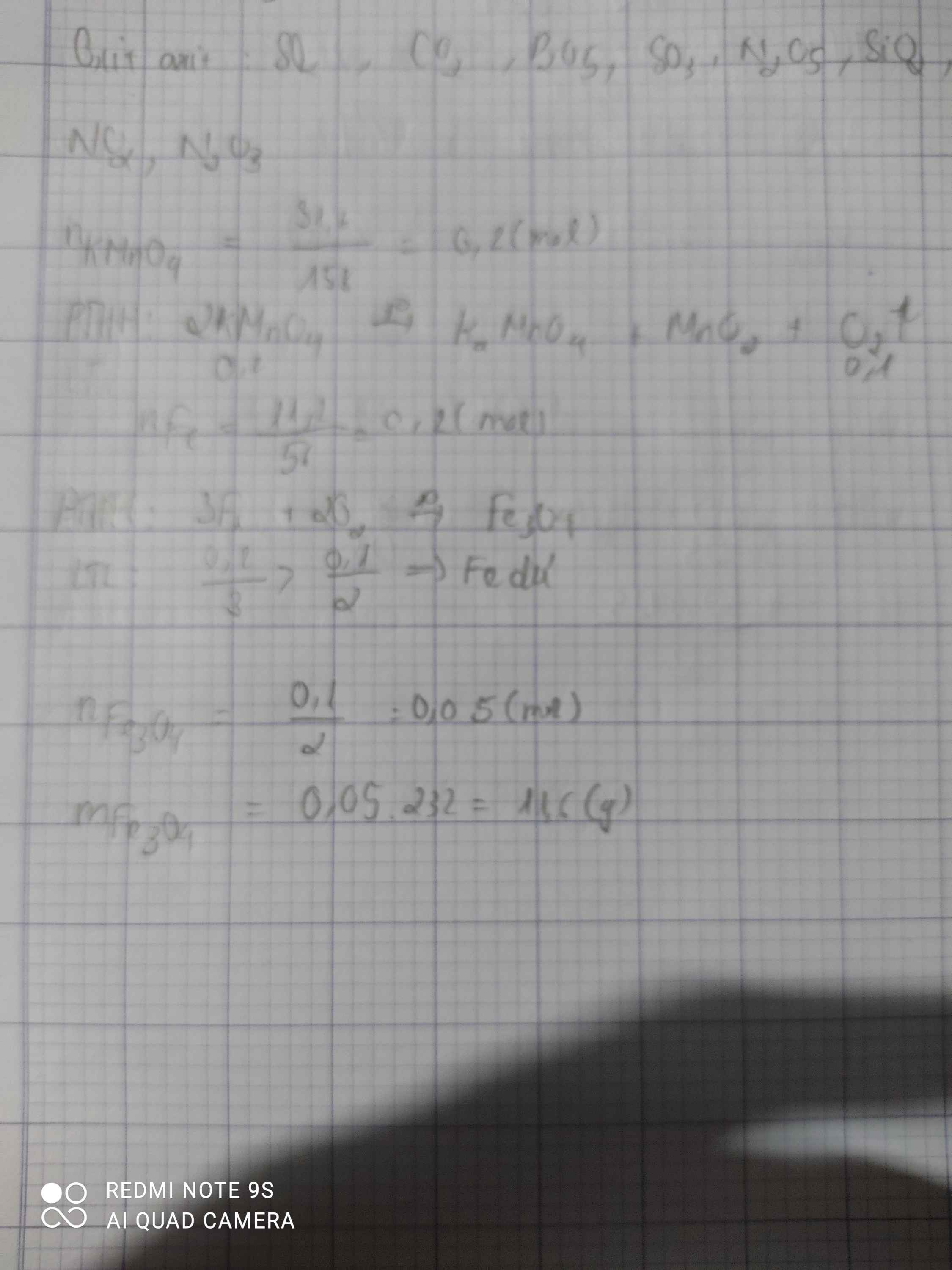

không vì nó kết hợp vs O2 tạo ra oxit
Bài 1:
Bài 2:
a) AgNO3
CTHH AgNO3 mang ý nghĩa:
- Là hợp chất tạo bởi 3 nguyên tố hóa học : Ag , N và O
- Tạo bởi 1 nguyên tử nguyên tố Ag, 1 nguyên tử nguyên tố N và 3 nguyên tử nguyên tố O.
- \(PTK_{AgNO_3}=NTK_{Ag}+NTK_N+3.NTK_O\\ =108+14+3.16=170\left(đ.v.C\right)\)
b) KHSO4
CTHH KHSO4 mang ý nghĩa:
- Là hợp chất cấu tạo từ 4 nguyên tố hóa học: K,H,S và O
- Cấu tạo bởi 1 nguyên tử nguyên tố K, 1 nguyên tử nguyên tố H, 1 nguyên tử nguyên tố A và 4 nguyên tử nguyên tố O.
- \(PTK_{KHSO_4}=NTK_K+NTK_H+NTK_S+4.NTK_O\\ =39+1+32+4.16=136\left(đ.v.C\right)\)
Bài tập 3:
a) Gọi CT ghi hóa trị của S(IV) và O là \(S_x^{IV}O_y^{II}\)(x,y : nguyên, dương)
Theo quy tắc hóa trị, ta có:
\(x.IV=y.II\\ =>\dfrac{x}{y}=\dfrac{II}{IV}=\dfrac{2}{4}=\dfrac{1}{2}\)
=> x=1; y=2
=> CTHH là SO2
b) Gọi CT ghi hóa trị của Al(III) và Cl(I) là \(Al_x^{III}Cl_y^I\) (x,y: nguyên, dương)
Theo quy tắc hóa trị ta có:
\(x.III=y.I\\ =>\dfrac{x}{y}=\dfrac{I}{III}=\dfrac{1}{3}\)
=> x=1; y=3
=> CTHH là AlCl3
Bài 4:
a) Gọi CT gọi hóa trị của hợp chất CuCl2 là \(Cu^aCl_2^b\)(a,b: nguyên, dương)
Theo Quy tắc hóa trị, ta có:
\(1.a=2.b\\ =>\dfrac{a}{b}=\dfrac{2}{1}=\dfrac{II}{I}\)
=> a= II, b=I
=> Trong hợp chất CuCl2 : Cu(II) và Cl(I)
b) Gọi CT kèm hóa trị của hợp chất Fe(NO3)2 là: \(Fe^a\left(NO_3\right)_2^b\) (a,b: nguyên, dương)
Theo quy tắc hóa trị, ta có:
\(1.a=2.b\\ =>\dfrac{a}{b}=\dfrac{2}{1}=\dfrac{II}{I}\\ =>a=II;b=I\)
=> Trong hợp chất Fe(NO3)2 : Fe(II) và nhóm nguyên tử NO3 (I)