Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Số mol nHCl = 0,04 mol ⇒ nOH– = 0,04 mol.
⇒ Bảo toàn điện tích ta có: nNa+ = 0,03 mol.
⇒ Chất rắn thu được khi cô cạn dd X = 0,01×137 + 0,01×62 + 0,04×17 + 0,03×23 = 3,36 gam.

Đáp án C
Số mol nHCl = 0,04 mol ⇒ nOH– = 0,04 mo.
⇒ Bảo toàn điện tích ta có: nNa+ = 0,03 mol.
⇒ Chất rắn thu được khi cô cạn dd X = 0,01×137 + 0,01×62 + 0,04×17 + 0,03×23 = 3,36 gam.

Đáp án B
• X có dạng H2NR(COOH)b
• 0,01 mol H2NR(COOH)b + 0,02 mol NaOH
nNaOH = 2 × n H2NR(COOH)b → b = 2 → X là H2NR(COOH)2
• 0,03 mol H2NR(COOH)2 + 0,0705 mol NaOH → 6,15 gam rắn
Ta có hỗn hợp rắn gồm muối 0,03 mol H2NR(COONa)2 và 0,0105 mol NaOH dư → mH2NR(COONa)2 = 6,15 - 0,0105 × 40 = 5,73 gam.
MH2NR(COONa)2 = 16 + MR + 2 × 67 = 5,73 : 0,03 → MR = 41 → R là -C3H5- → X là H2NC3H5(COOH)2

Đáp án D
BTĐT: nNO3- = nNa+ + 2nBa2+ + 2nMg2+ - nCl- = 0,3.1+0,1.2+0,05.2-0,2.1=0,4 mol
m muối = mNa+ + mBa2+ + mMg2+ + mCl- + mNO3-
= 0,3.23+0,1.137+0,05.24+0,2.35,5+0,4.62 = 53,7 gam

Đáp án C
Có dung dịch X gồm NaCl (0,12 mol), và (NH4)2SO4 (0,025 mol)
(NH4)2SO4 + Ba(OH)2 → BaSO4 + 2NH3 + 2H2O
Sau phản ứng dư: 0,005 mol Ba(OH)2 trong dung dịch
m= 0,12.58,5 + 0,005.171 = 7,875 gam

Đáp án B
Nếu n HCO 3 - ≤ 2 n Ba 2 + thì khi cô cạn dung dịch X và nung đến khối lượng không đổi sẽ thu được hỗn hợp gồm BaO, NaCl hoặc BaO, NaCl và BaCl2. Như vậy, ion HCO 3 - đã được thay bằng ion O 2 - . Theo giả thiết và bảo toàn điện tích, ta có :
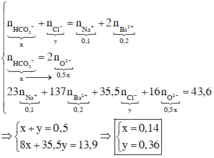
Nếu trường hợp ![]() không thỏa mãn thì ta xét trường hợp
không thỏa mãn thì ta xét trường hợp ![]() . Khi đó chất rắn sẽ gồm Na2CO3, BaO và NaCl.
. Khi đó chất rắn sẽ gồm Na2CO3, BaO và NaCl.

Theo BTĐT: x = (0,12 + 0,05 – 0,12) : 2 = 0,025 mol.
Cho 0,03 mol Ba(OH)2 phản ứng với ddX
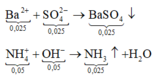
Vậy khi phản ứng xảy ra hoàn toàn, lọc bỏ kết tủa thu được ddY gồm 0,12 mol Na+; 0,12 mol Cl−; 0,005 mol Ba2+; 0,01 mol OH−
Vậy m = 0,12x23 + 0,12x35,5 + 0,005x137 + 0,01x17 = 7,875 gam
Đáp án A

Đáp án B
Ta có các phản ứng:
ClH3NCH2COOH + 2NaOH → H2NCH2COONa + NaCl + 2H2O
CH3CH(NH2)COOH + NaOH → CH3CH(NH2)COONa + H2O
HCOOC6H5 + 2NaOH → HCOONa + C6H5ONa + H2O
+ Nhận thấy ∑nH2O = 0,01×2 + 0,02 + 0,05 = 0,09 ⇒ mH2O = 1,62 gam
⇒ BTKL có mChất rắn = mClH3NCH2COOH + mCH3CH(NH2)COOH + mHCOOC6H5 + mNaOH – mH2O
⇔ mChất rắn = 13,775 gam ⇒ Chọn B (Chú ý NaOH có dư)

Đáp án B
Lời giải chi tiết
Để trung hòa ½ dung dịch X cần 0,02 mol HCl nên số mol OH- trong X là 0,04 mol hay a=0,04
Bảo toàn điện tích: b = 0,04 + 0,01 - 0,01.2 = 0,03
=> m = 0,01.137 + 0,01.62 + 0,04.17 + 0,03.23 = 3,36 gam