Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Dể ion Yn- tồn tại được trong dung dịch X thì Yn- không phản ứng với 3 ion còn lại => loại đáp án A và C.
Dung dịch X trung hòa điện tích nên: nK++2nBa2+=nHCO3-+a.n
0,01.1+0,02.2=0,02.1+n.a=>n.a=0,03. Với n=1 thì a=0,03.

Đáp án A
Theo ĐLBT ĐT có: dung dịch chứa Ba2+ 0,02 mol, OH- 0,06 mol và Na+ 0,02 mol với dung dịch chứa HCO3- 0,04 mol ; CO32- 0,03 mol và Na+ 0,1 mol
HCO3-+ OH-→ CO32-+ H2O
0,04 0,06 0,04 mol
Ba2++ CO32-→ BaCO3
0,02 0,07 0,02 mol
suy ra mBaCO3 = 0,02.197 = 3,94 gam

Đáp án A
TH1: Ion X có điện tích= -1 ⇒ nX = 0,01 + 0,02×2 – 0,02 = 0,03
⇒ chọn A hoặc D
Loại D vì OH- và HCO3- không cùng tồn tại trong cùng 1 dung dịch
Đáp án A.
TH2: Ion X có điện tích = -2 ⇒ nX = (0,01 + 0,02×2 – 0,02): 2 = 0,015 ( Không thỏa mãn đáp án)

Đáp án A
Mg(NO3)2 →Mg2+ + 2NO3-
0,03 mol 0,06 mo
Al2(SO4)3 →2Al3+ + 3SO42-
0,06 0,09 mol

Đáp án A
Để dung dịch X tồn tại thì Y là NO3- hoặc Cl-
Ta thấy có đáp án A thỏa mãn định luật bảo toàn điện tích:
0,01.1 + 0,02.2 = 0,02.1 + 0,03.1

Đáp án D
Bảo toàn điện tích: ax = 0,01 + 0,02 x 2 - 0,02 = 0,03
Chỉ có D thõa mãn; vì OH- không tồn tại chung dung dịch với HCO3-
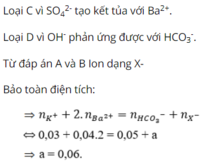
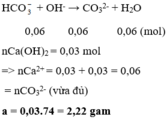

Đáp án B