Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\overline{M}=24\cdot2=48\)
\(\dfrac{n_{SO_2}}{n_{O_2}}=\dfrac{64-48}{48-32}=1\)
\(n_{hh}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(\Rightarrow n_{SO_2}=n_{O_2}=0.15\left(mol\right)\)
\(2SO_2+O_2\underrightarrow{^{t^0,V_2O_5}}2SO_3\)
Bđ:0.15....0.15
Pư: x..........0.5x......x
KT: 0.15-x..0.15-0.5x..x
\(n_{hh}=0.15-x+0.15-0.5x+x=0.3-0.5x\left(mol\right)\)
\(m=\left(0.15-x\right)\cdot64+\left(0.15-0.5x\right)\cdot32+80x=\left(0.3-0.5x\right)\cdot2\cdot26\)
\(\Rightarrow x=\dfrac{3}{65}\)
\(H\%=\dfrac{\dfrac{3}{65}}{0.15}\cdot100\%=30.7\%\)

Ta có :
\(m_{hỗn\ hợp} = n.M = \dfrac{2,24}{22,4}.2.7,56 = 1,521(gam)\)
Bảo toàn khối lượng , sau khi nung : m = 1,521(gam)
\(\Rightarrow n_{hỗn\ hợp\ sau} = \dfrac{1,521}{2.8,4} = 0,09(mol)\)
Ta có :
\(\dfrac{p_{trước}}{p_{sau}} = \dfrac{n_{trước}}{n_{sau}}\)
⇔ \(\dfrac{1}{p_{sau}} = \dfrac{0,1}{0,09}\\ \Rightarrow p_{sau} = 0,9\ atm\)

Ta có MX = 3,6.2 =7,2.
Áp dụng qui tắc đường chéo :
=> nH2 : nN2 = 4 : 1
Đặt nH2 = 4 mol => nN2 = 1 mol
N2 + 3H2 ---> 2NH3
x----->3x-------->2x
=> nY = 5 – 2x mol
Bảo toàn khối lượng :
mX = mY = 4.2 + 1.28 = 36g
=> MY = 4.2 = \(\dfrac{36}{5-2x}\)
=> x = 0,25 mol
Tính hiệu suất theo N2 => H = \(\dfrac{0,25}{1}\)= 25%

a) \(M_{hh}=0,6.29=17,4\) (g/mol)
Dùng phương pháp đường chéo :
=> Trong 3 lít hỗn hợp trên \(\left\{{}\begin{matrix}2,7\left(lít\right)CH_4\\0,3\left(lít\right)C_2H_6\end{matrix}\right.\)
PTHH : \(CH_4+2O_2-t^o->CO_2+2H_2O\) (1)
\(C_2H_6+\dfrac{7}{2}O_2-t^o->2CO_2+3H_2O\) (2)
Theo pthh (1) và (2) : \(\Sigma n_{O2}=2n_{CH4}+\dfrac{7}{2}n_{C2H6}\)
=> \(\Sigma_{V_{O2}}=2V_{CH4}+\dfrac{7}{2}V_{C2H6}=6,45\left(l\right)\)
b) HD : Áp dụng ĐLBTKL : mhh + mo2 = msp.cháy

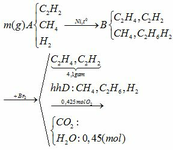
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)

Chọn nCO2 = 6 , nH2O = 7
Hỗn hợp Y gồm nO2 = a mol, nO3 = b mol
X + Y → CO2 + H2O
Áp dụng ĐLBT nguyên tố O: 2a + 3b = 6.2 + 7
mY = 32a + 48b = 19.2 (a+b)
=> a = 5 và b = 3
=> nX = 1/2 nY = 4 mol
=> mX = 6.44 + 7.18 - 32.5 - 48.3 = 83 gam
<=> MX = \(\dfrac{m_X}{n_X}\)= 20,75 gam/mol
<=> d\(\dfrac{X}{H_2}\)= 20,75:2 = 10,375

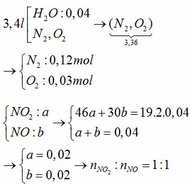
Tỉ lệ mol của 2 khí NO2 và NO là 1:1, khí O2 không đủ nên giả sử mol pứ đều là: x (mol)
2NO2 + ½ O2 + H2O → 2HNO3
x→ 0,25x x
2NO + 1,5O2 + H2O → 2HNO3
x → 0,75x x
pứ: x 2x
nO2 = 0,03 => x = 0,03
=> nHNO3 = 0,06
mbình sau pứ = N2 + mO2 + mH2O+ mNO2 + mNO = 28 . 0,12 + 32 . 0,03 + 40 + 19 . 2 . 0,04 = 45,84g
=> %HNO3 = 8,246%
