
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


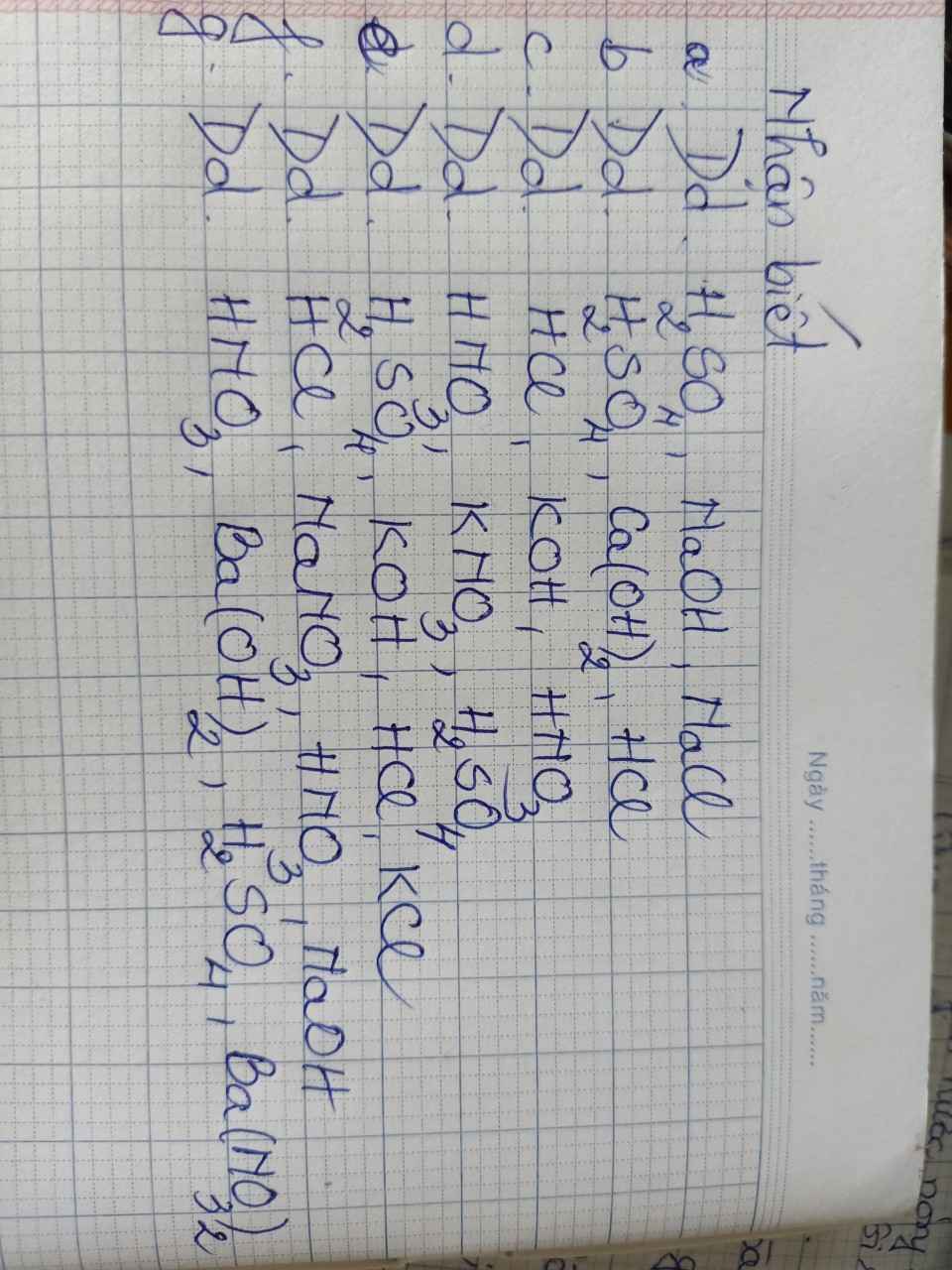
a) - Dùng quỳ tím:
+ Hóa đỏ -> dd H2SO4
+ Hóa xanh -> dd NaOH
+ Không đổi màu -> dd NaCl
b) - Dùng quỳ tím:
+ Hóa xanh -> dd Ca(OH)2
+ Hóa đỏ -> dd H2SO4, dd HCl
- Dùng dd BaCl2:
+ Có kết tủa trắng BaSO4 -> dd H2SO4
+ Không có kt trắng -> dd HCl
PTHH: H2SO4 + BaCl2 -> BaSO4 (kt trắng) + 2 HCl

a) \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right);n_{H_2SO_4}=0,1.2,5=0,25\left(mol\right)\)
PTHH: Zn + H2SO4 → ZnSO4 + H2
Mol: 0,2 0,2 0,2 0,2
Ta có: \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\) ⇒ Zn hết, H2SO4 dư
b) \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c) \(m_{ZnSO_4}=0,2.161=32,2\left(g\right)\)
\(m_{H_2SO_4\left(dư\right)}=\left(0,25-0,2\right).98=4,9\left(g\right)\)
Bài 2 :
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
100ml = 0,1l
\(n_{H2SO4}=2,5.0,1=0,25\left(mol\right)\)
a) Pt : \(Zn+2H_2SO_4\rightarrow ZnSO_4+H_2|\)
1 1 1 1
0,2 0,25 0,2 0,2
b) Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,25}{2}\)
⇒ Zn phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của Zn
\(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
c) \(n_{ZnCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(n_{H2SO4\left(dư\right)}=0,25-0,2=0,05\left(mol\right)\)
⇒ \(m_{H2SO4\left(dư\right)}=0,05.98=4,9\left(g\right)\)
Chúc bạn học tốt

a)\(2Ca+O_2\underrightarrow{t^o}2CaO\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
\(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
\(CaO+2HCl\rightarrow CaCl_2+H_2O\)

Bài 1:
\(n_{CuO}=\dfrac{56}{80}=0,7\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: 0,7 1,4
\(m_{ddHCl}=\dfrac{1,4.36,5.100}{14,6}=350\left(g\right)\)
Bài 2:
\(n_{Na_2SO_3}=\dfrac{12,6}{126}=0,1\left(mol\right)\)
PTHH: Na2SO3 + 2HCl → 2NaCl + SO2 + H2O
Mol: 0,1 0,1
\(V_{SO_2}=0,1.22,4=2,24\left(l\right)\)

a) CuO + 2HCl → CuCl2 + H2O (1)
ZnO + 2HCl → ZnCl2 + H2O (2)
b) Gọi số mol CuO, ZnO lần lượt là x, y
mhh = mCuO + mZnO → 80x + 81y = 12,1 (*)
nHCl = 0,1 . 3 = 0,3 mol
Theo (1): nHCl (1) = 2nCuO = 2x
Theo (2): nHCl (2) = 2nZnO = 2y
nHCl = 2x + 2y = 0,3 (**)
Từ (*) và (**) → x = 0,05; y = 0,1
%mCuO=0,05.8012,1.100%=33,06%%mZnO=100%−33,06%=66,94%%mCuO=0,05.8012,1.100%=33,06%%mZnO=100%−33,06%=66,94%
c) CuO + H2SO4 → CuSO4 + H2O
0,05 → 0,05
ZnO + H2SO4 → ZnSO4 + H2O
0,1 → 0,1
nH2SO4 = 0,05 + 0,1 = 0,15 mol
mH2SO4 = 0,15 . 98 = 14,7g
mdd H2SO4 = 14,7 : 20% = 73,5(g)
cho mik xin 1 like zới đc khum:))

a)
4Na + O2 ---to→ 2Na2O
Na2O + H2O → 2NaOH
2NaOH + CO2 → Na2CO3 + H2O
Na2CO3 + Ca(OH)2 → 2NaOH + CaCO3
CaCO3 ---to→ CaO + CO2
CO2 + NaOH → NaHCO3
NaHCO3 + H2SO4 → Na2SO4 + CO2 + H2O
Na2SO4 + Ba(OH)2 → 2NaOH + BaSO4
b)
S + O2 ---to→ SO2
2SO2 + O2 ---to(V2O5)→ 2SO3
SO3 + H2O → H2SO4
H2SO4 + Cu(OH)2 → CuSO4 + 2H2O
CuSO4 + FeCl2 → CuCl2 + FeSO4
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
Fe(OH)2 + 2HCl → FeCl2 + 2H2O
2FeCl2 + Cl2 → 2FeCl3
2FeCl3 + 3Ba(OH)2 → 2Fe(OH)3 + 3BaCl2
2Fe(OH)3 ---to→ Fe2O3 + 3H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O

bài 28 ý hả bn! bn nêu đề ra nha!
mk dùng sách vnen nên ko có mấy cái đó.








43.a) \(m_{HCl\left(bđ\right)}=200.10,95\%=21,9\left(g\right)\)
=> \(n_{HCl\left(bđ\right)}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
b) HCl phản ứng với NaOH là HCl dư
\(HCl+NaOH\rightarrow NaCl+H_2O\)
\(n_{HCl\left(dư\right)}=n_{NaOH}=0,05.2=0,1\left(mol\right)\)
=> \(n_{HCl\left(pứ\right)}=n_{HCl\left(bđ\right)}-n_{HCl\left(dư\right)}=0,6-0,1=0,5\left(mol\right)\)
c) \(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
\(n_{CaCO_3}=\dfrac{1}{2}n_{HCl\left(pứ\right)}=0,25\left(mol\right)\)
=> \(m_{CaCO_3}=0,25.100=25\left(g\right)\)
d) \(n_{CO_2}=\dfrac{1}{2}n_{HCl\left(pứ\right)}=0,25\left(mol\right)\)
=> \(V_{CO_2}=0,25.22,4=5,6\left(l\right)\)
e) \(m_{ddsaupu}=25+200-0,25.44=214\left(g\right)\)
Dung dịch A gồm CaCl2 và HCl dư
\(n_{CaCl_2}=\dfrac{1}{2}n_{HCl\left(pứ\right)}=0,25\left(mol\right)\)
\(C\%_{CaCl_2}=\dfrac{0,25.111}{214}.100=12,97\%\)
\(C\%_{HCl\left(dư\right)}=\dfrac{0,1.36,5}{214}.100=1,71\%\)