
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Mỗi một câu trong mỗi phần mình đánh số (1),(2),... nhé
a)
(1) : Biến đổi vật lí
(2) : Biến đổi hóa học
b)
(1) : Biến đổi vật lí
(2) : Biến đổi hóa học
a) Giũa một đinh sắt thành mạt sắt => Biến đổi vật lý
Ngâm mạt sắt trong ống nghiệm đựng axit clohidric, thu được sắt clorua và khí hidro => Biến đồi hóa học
Fe + 2HCl --------> FeCl2 + H2
b) Cho một ít đường vào ống nghiệm đựng nước, khuấy cho đường tan hết ta thu được nước đường =>Biến đổi vật lý
Đun sôi nước đường trên ngọn lửa đèn cồn, nước bay hơi hết => Biến đổi vật lý
Tiếp tục đun ta được chất rắn màu đen và khí thoát ra, khí này làm đục nước vôi trong => Biến đồi hóa học
C12H22O11 + 12O2 ------> 12CO2 + 11H2O
CO2 + Ca(OH)2 ------> CaCO3 + H2O


a. \(PTHH:3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\)
b. \(n_{Fe_2O_3}=\dfrac{m_{Fe_2O_3}}{M_{Fe_2O_3}}=\dfrac{4}{160}=0,025\left(mol\right)\)
\(PTHH:3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\)
Mol : 3 : 1 : 2 : 3
Mol : 0,075 ← 0,025 → 0,05 → 0,075
\(\Rightarrow n_{H_2}=0,075\left(mol\right)\)
\(\Rightarrow V_{H_2}=n_{H_2}.22,4=0,075.22,4=1,68\left(l\right)\)
c. Từ câu b. \(\Rightarrow n_{Fe}=0,05\left(mol\right)\)
\(\Rightarrow m_{Fe}=n_{Fe}.M_{Fe}=0,05.56=2,8\left(g\right)\)

Câu 18
Số mol S=8/32=0,25mol
Số nguyên tử S là 0,25.6,022.10^23=1,5055.10^23 nguyên tử
Số nguyên tử Na=2.1,5055.10^23=3,011.10^23 ngtu
Số mol Na là n= 3,11.10^23/(6,022.10^23)=0,5mol
m(Na)=0,5.23=11,5g

a)
\(n_{N_2}=\dfrac{m}{M}=\dfrac{0,28}{28}=0,01\left(mol\right)\)
\(V_{N_2\left(dktc\right)}=n\cdot22,4=0,01\cdot22,4=0,224\left(l\right)\)
b)
\(n_{CuCl_2}=\dfrac{0,3\cdot10^{23}}{6\cdot10^{23}}=0,05\left(mol\right)\\ m_{CuCl_2}=0,05\cdot\left(64+71\right)=6,75\left(g\right)\)
\(m_{ZnCl_2}=n\cdot M=0,2\cdot\left(65+71\right)=27,2\left(g\right)\)

Câu 8:
a) Bảo toàn khối lượng: \(m_{O_2}=m_{KClO_3}-m_{rắn}=9,6\left(g\right)\)
\(\Rightarrow n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\) \(\Rightarrow V_{O_2}=0,3\cdot22,4=6,72\left(l\right)\)
b) Bảo toàn khối lượng: \(m_{rắn}=m_{O_2}+m_P=9,6+9,3=18,9\left(g\right)\)

Gọi x,y là số mol của Al , Mg
a.2Al + 3H2SO4 ----> Al2(SO4)3 + 3H2
x _______________________ 3/2x
4Mg + 5H2SO4 ---> 4MgSO4 + H2
y______________________ 1/4y
b. Số mol của H2 là
\(^nh2=\)\(\dfrac{V}{22,4}\) = \(\dfrac{8,96}{22,4}\) = 0,4 (mol)
\(\dfrac{3}{2}\)x + \(\dfrac{1}{4}\)y = 0,4 ⇒ x = 0,195
27x + 24y =15,6 y= 0,43
\(^mAl=\) 0,195 . 27 = 5,265 (g)
\(^mMg=\) 0,43 . 24 = 10,32 (g)
%\(^mAl\) = \(\dfrac{5,256.100\%}{15,6}\)= 33,.75%
\(^{\%m}Mg=\)100% - 33,75% = 66,25%

a) \(n_{Fe}=\dfrac{28}{56}=0.5\left(mol\right)\)
\(n_{O_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\)
\(Bđ:0.5....0.2\)
\(Pư:0.3.....0.2........0.1\)
\(Kt:0.2.......0..........0.1\)
\(m_{Fe\left(dư\right)}=0.2\cdot56=11.2\left(g\right)\)
\(m_{Fe_3O_4}=0.1\cdot232=23.2\left(g\right)\)
a. \(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
\(n_{O_2}=\dfrac{4.48}{22,4}=0,2\left(mol\right)\)
Ta thấy : 0,5 > 0,2 => Fe dư , O2 đủ
PTHH : 3Fe + 2O2 ---to---> Fe3O4
0,3 0,2 0,1
\(m_{Fe\left(dư\right)}=\left(0,5-0,3\right).56=11,2\left(g\right)\)
b. \(m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\)

 Mb đang onl giúp mik vs nha! Cần gấp Y_Y !!!
Mb đang onl giúp mik vs nha! Cần gấp Y_Y !!!
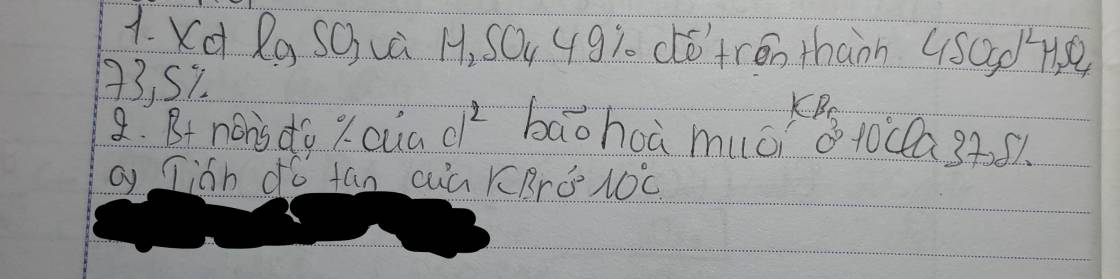 giải giúp mik vs ạ mik đang cần gấp!!!
giải giúp mik vs ạ mik đang cần gấp!!!
 các bn bỏ bài 16 , 17 , 21 nha Còn giúp mik vs nha mik đg cần gấp
các bn bỏ bài 16 , 17 , 21 nha Còn giúp mik vs nha mik đg cần gấp

 GIÚP MIK VỚI Ạ!! MIK ĐANG CẦN GẤP
GIÚP MIK VỚI Ạ!! MIK ĐANG CẦN GẤP
Câu 6:a)\(Fe+2HCl\rightarrow FeCl_2+H_2\)
b)\(n_{H_2}:\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
1...............2...........................1(mol)
0,25...........0,5,,,,,,,,,,,,,,,,,,,,,,0,25(mol)
\(m_{Fe}:56.0,25=14\left(g\right)\)
c)\(m_{HCl}:36,5.0,5=18,25\)
d)\(n_{CuO}:\dfrac{8}{80}=0,1\left(mol\right)\)
\(H_2+CuO\rightarrow Cu+H_2O\)
1.............1...........1..............(mol)
0,1........0,1..........0,1............(mol)
=>Hidro dư
\(m_{Cu}:0,1.64=6,4\left(g\right)\)
Câu 5:
a)\(Mg+2HCl\rightarrow MgCl_2+H_2\)
b)\(n_{Mg}:\dfrac{3,6}{24}=0,15\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
1..............2...............1.............1(mol)
0,15..........0,3............0,15.......0,15(mol)
\(m_{MgCl_2}:0,15.95=14,25\left(g\right)\)
\(V_{H_2}:0,15.22,4=3,36\left(l\right)\)
c)\(m_{HCl}:0,3.36,5=10,95\left(g\right)\)
d)\(n_{CuO}:\dfrac{16}{80}=0,2\left(mol\right)\)
\(H_2+CuO\rightarrow Cu+H_2O\)
1.............1..........1..............(mol)
0,15........0,15......0,15.........(mol)
\(m_{Cu}:0,15.65=9,75\left(g\right)\)
\(m_{CuO}dư:\left(0,2-0,15\right).80=4\left(g\right)\)