Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

KClO3 vừa có tính oxi hóa vừa có tính khử
(1) KClO3 (O-2 → O0)
(2) KClO3 (O+5 → O+7)

Đáp án C
MnO2 là chất xúc tác nên sử dụng định luật bảo toàn khối lượng ta được:
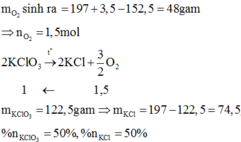

Đáp án B
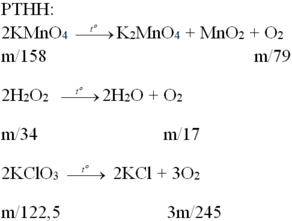
PTHH:
2KMnO4 K2MnO4 + MnO2 + O2
2H2O2 → 2H2O + O2
2KClO3 → 2KCl + 3O2
đây là lượng số mol phải không ạ?
còn cùng khối lượng thì H2O2 nhiều hơn phải không ạ?

Đáp án A
Số mol K2Cr2O7 là: n K 2 Cr 2 O 7 = 0 , 02 mol
Sơ đồ phản ứng: K 2 Cr 2 + 6 O 7 ⏟ chất oxi hóa + H C l - 1 ⏟ c h ấ t k h ử v à m ô i t r ư ờ n g → K C l - 1 + C r + 3 C l 3 - 1 + C l 2 0 + 2 H 2 O
Theo sơ đồ phản ứng thì HCl bị oxi hoá sẽ chuyển hết về Cl2. Bảo toàn mol electron ta có:
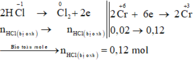

Gọi x là số mol KCl O 3 bị phân huỷ theo (a).
Gọi y là số mol KCl O 3 bị phân huỷ theo (b).
2KCl O 3 → 2KCl + 3 O 2
4KCl O 3 → 3KCl O 4 + KCl
Ta có x + y = 73,5/122,5 = 0,6 (1)
x + y/4 = 33,5/74,5 = 0,45 (2)
Từ (1) và (2) , giải ra:
x =0,4 → phần trăm KCl O 3 bị phân hủy theo (a) là: 0,4/0,6 x 100 % = 66,66%
y =0,2 → phần trăm KCl O 3 bị phân hủy theo (b) là: 0,2/0,6 x 100 % = 33,34%