Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
nCuCO3 = nCO2 = 0,11 mol
nNa2SO3 = nSO2 = 0,14 mol
Thể tích dung dịch axit là x lít => nHCl = x và nH2SO4 = 0,5x => nH2O = x
BTKL:36,5x+98.0,5x+m=m+8,475+0,25.55,2+18x => x = 0,33
Dung dịch Y chứa SO42- (0,165), Cl- (0,33), Na+ (0,28) => nCu2+ = 0,19 => nCuO = 0,08
=> m = 37,68 và nFe = 0,0942
nCu2+ bị đp = 0,19.94% = 0,1786
=> n e trao đổi = nCl- + 4nO2 => nO2 = 0,068
=> nH+ = 4nO2 = 0,0272
Fe với dung dịch Z: nFe pư = nCu2+ + nH+/2 = 0,025
=> m1 = mFe dư + mCu = 4,6048 gam

Đáp án A
Nhận thấy, nFe2+(dd Y) = nNO2 – 2nH2 = 0,39 – 2.0,04 = 0,31 mol
Giả sử nHCl = 2a; nH2SO4 = a
nBaSO4 = a, nAgCl = 4a, nAg = nFe2+ = 0,31 => 233a + 143,5.4a + 0,31.108 = 211,02 => a = 0,22
BTNT H => nHCl + 2nH2SO4 = 2nH2 + 2nH2O => nH2O = (0,44 + 2.0,22 – 2.0,04)/2 = 0,4 mol
BTKL: m = mX + mHCl + mH2SO4 – mH2 – mH2O = 29,68 + 0,44.36,5 + 0,22.98 – 0,04.2 – 0,4.18 = 60,02 gam

Trong X có : nFe3O4 = 0,03 mol ; nCuO = 0,02 mol
Khi phản ứng với HCl vừa đủ thì trong dung dịch có :
0,02 mol Cu2+ ; 0,03 mol Fe2+ ; 0,06 mol Fe3+ ; 0,28 mol Cl- .
Khi điện phân :
+/ Anot : 2Cl- → Cl2 + 2e
+/ Catot : Fe3+ + 1e → Fe2+ (1)
Cu2+ + 2e → Cu (2)
Fe2+ + 2e → Fe (3)
Nếu dung dịch chỉ giảm khối lượng vì Cl2 bay ra , chỉ xảy ra (1) ở Catot
=> ne trao đổi = 0,06 mol => mCl2 = 2.13g < 11,18g =>Loại
Nếu (10 và (20 xảy ra vừa đủ => ne trao đổi = 0,1 mol
=> mgiảm = mCl2 + mCu = 4,83g < 11,18 =>Loại
Vậy xảy ra cả (1) ; (2) ; (3)
Đặt nFe2+ phản ứng = a mol
=> ne trao đổi = (0,1 + 2a) mol => nCl2 = (0,05 + a) mol
=>mGiảm = 0,02.64 + 56a + 71.(0,05 + a) = 11,18
=> a = 0,05 mol
=>nFe2+ dư = 0,03 + 0,06 – 0,05 = 0,04 mol
Khi phản ứng với KMnO4 tạo MnSO4 ; Fe2+ bị OXH thành Fe3+
Bảo toàn e : nFe2+ = 5nKMnO4 => 0,04 = 5.0,1V
=>V = 0,08 l = 80 ml
=>B

Đáp án A
Hòa tan hết 7,44 gam hỗn hợp rắn vào 0,4 mol HCl và 0,05 mol NaNO3 thu được 22,47 gam muối và 0,02 mol hỗn hợp khí gồm NO và N2.
Giải được số mol NO và N2 đều là 0,01 mol.
Do X chứa muối nên HCl phản ứng hết.
BTKL: m H 2 O = 7 , 44 + 0 , 4 . 36 , 5 + 0 , 05 . 85 - 22 , 47 - 0 , 02 . 29 = 3 , 24 → n H 2 O = 0 , 18
BTNT H: n N H 4 + = 0 , 4 - 0 , 18 . 2 4 = 0 , 01 m o l
Cho NaOH dư vào X thu được kết tủa Y, nung Y trong không khí thu được rắn chứa MgO và Fe2O3 có khối lượng 9,6 gam.
Lượng O để oxi hóa hỗn hợp ban đầu lên tối đa là: n O = 9 , 6 - 7 , 44 16 = 0 , 135 m o l
Cho AgNO3 dư tác dụng với dung dịch X ta thu được kết tủa gồm AgCl 0,4 mol (bảo toàn C) và Ag.
Bảo toàn e:
n A g = 0 , 135 . 2 - 0 , 01 . 8 - 0 , 01 . 3 - 0 , 01 . 10 = 0 , 06 m o l → m = 63 , 88 g a m

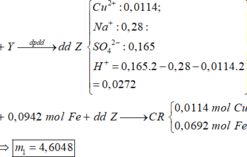

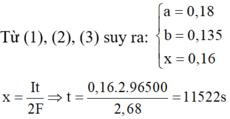






Đáp án D
Khí gồm SO2 ; CO2 có n = 0,25 mol và M = 55,2g
=> nSO2 = 0,14 ; nCO2 = 0,11 mol
=> nNa2SO3 = 0,14 ; nCuCO3 = 0,11
Gọi thể tích dung dịch axit là V => nHCl = V ; nH2SO4 = 0,5V mol
=> nH2O =1/2 nH+ = V mol
Bảo toàn khối lượng : mX + maxit = mchất tan + mkhí + mH2O
=> V = 0,33 lit
=> nHCl = 0,33 ; nH2SO4 = 0,165 mol
Bảo toàn điện tích : nNa+ + 2nCu2+ = nCl- + 2nSO4 => nCu2+ = 0,19 mol
=> nCuO = 0,19 – 0,11 = 0,08 mol => m = 37,68g
, nCu2+ đp = 0,19.0,94 = 0,1786 mol
Catot : Cu2+ + 2e -> Cu
Anot : 2Cl- -> Cl2 + 2e
2H2O -> 4H+ + O2 + 4e
=> 2nCu2+ đp = nCl- + nH+ => nH+ = 0,0272 mol
Lấy nFe = 0,0942 mol phản ứng với Z( 0,0272 mol H+ và 0,0114 mol Cu2+)
=> sau phản ứng có : 0,0114 mol Cu và 0,0692 mol Fe dư
=> m1 = 4,6048g
=>D