Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
![]()
![]()
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
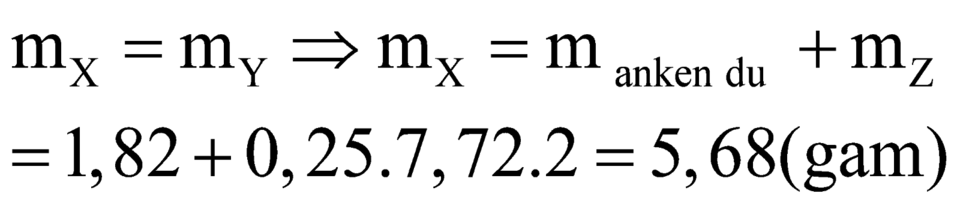
Mà ![]()
![]()
![]()
Do đó hai anken trong X là C2H4 và C3H6.
Cách 1: Áp dụng sơ đồ đường chéo hoặc giải hệ phương trình, ta có:
![]()
Cách 2: Ta có: ![]()
![]()
Vì ![]() nên
nên ![]()

nBr2 = 0,05
Dẫn hỗn hợp Y qua dung dịch Br2 dư thấy khối lượng bình tăng 1,82 gam và có 8 gam brom đã tham gia phản ứng
⇒ nAnken/Y = nBr2 = 0,05 = nC2H4 dư + nC3H6 dư (1)
mAnken/Y = 1,82g
Vì Hiệu suất hidro hóa của 2 anken như nhau
⇒ nC2H4 phản ứng : nC2H4 ban đầu = nC3H6 phản ứng : nC3H6 ban đầu
⇒ nC2H4 dư : nC2H4 = nC3H6 dư : nC3H6
⇒ nC2H4 dư : 0,1 = nC3H6 dư : 0,15 (2)
Từ (1) và (2) ⇒ nC2H4 dư = 0,02 ; nC3H6 = 0,03
nC2H4 phản ứng = 0,1 – 0,02 = 0,08
⇒ H = (0,08 : 0,1).100% = 80%
Đáp án B.

Đáp án B
nhh = 0,1 mol.
Giả sư: nC2H4 = nC3H6 = a mol → nH2 = 1 - 2a mol.
→ mX = 28a + 42a + 2(0,1 - 2a) = 15,2 x 0,1
→ a = 0,02 mol.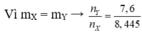
→ nY = 0,09 mol.
Ta có nH2phản ứng = nX - nY = 0,1 - 0,09 = 0,01 mol.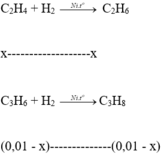
mbình tăng = (0,02 - x) x 28 + (0,02 - 0,01 + x) x 42 = 1,015
→ x = 0,0025 mol.

Đáp án B
Ta có nC2H2 = 0,04 mol, nH2 = 0,06 mol
Bảo toàn khối lượng → mX = m bình tăng + mZ
→ mbình tăng = 0,04.26 + 0,06.2-4,5.2.0,04 = 0,8 gam

Chọn đáp án C
Ta có:mX=0,15.16+ 0,09.26+0,2.2=5,14gam
+ Theo ĐLBTKlg: mX = mY + mZ ⇒ mZ = mX – mY = 5,14 – 0,82 = 4,32 gam.
+ Mà: dZ/H2 = 8 ⇒ MY = 16/
⇒ nZ = mZ ÷ MZ = 4,32 ÷ 16 = 0,27 mol
⇒Thể tích của hh Z: V = 0,27 × 22,4 = 6,048 lít
⇒ Chọn C

Số mol các chất trong A là: 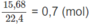
Khi A qua chất xúc tác Ni :
Hỗn hợp B chứa 3 chất: ankan ban đầu
C
n
H
2
n
+
2
, ankan mới tạo ra
C
m
H
2
m
+
2
và anken còn dư
C
m
H
2
m
với số mol tổng cộng là : 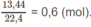
Số mol H 2 trong A là: 0,7 - 0,6 = 0,1(mol).
Khi B qua nước brom thì anken bị giữ lại hết:
C m H 2 m + B r 2 → C m H 2 m B r 2
Hỗn hợp C chỉ còn
C
n
H
2
n
+
2
và
C
m
H
2
m
+
2
với tổng số moi là 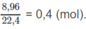
Như vậy, 0,2 mol C m H 2 m có khối lượng 5,6 g, do đó 1 mol C m H 2 m có khối lượng 28 (g) ⇒ m = 2.

Chọn đáp án D
Ta có mZ = 0,2 × 8,5×2 = 3,4 gam.
Ta có sơ đồ

+ Theo định luật BTKL ⇒ mC2H2 + mH2 = 19 + 3,4 = 22,4 gam
⇒ nC2H2 = nH2 = 22,4 ÷ (26 + 2) = 0,8 mol
+ Vì thành phần nguyên tố C và H trong X và Y như nhau.
⇒ Đốt cháy hoàn toàn hh Y hay X thì đều cần 1 lượng oxi như nhau.
Ta có sơ đồ đốt cháy
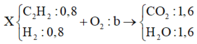
⇒nO2 = b = nCO2 + ½ nH2O = 2,4 mol ⇒ VO2 = 53,76 lít ⇒ Chọn D
Đáp án A
Vì nH2phản ứng = nanken phản ứng = nankan
→ nZ = nH2dư + nankan = nH2ban đầu = 0,25 mol.
→ nanken ban đầu = 0,4 - 0,25 = 0,15 mol.
Gọi x = nCnH2n + 2 → nH2dư = 0,25 - x (mol)
→ mZ = (14n + 2)x + 2(0,25 - x) = 0,25 x 7,72 x 2
→ 14nx = 3,36 (1)
nCnH2ndư = 0,15 - x → 14n(0,15 - x) = 1,82 (2)
Từ (1), (2) → x = 0,01; n = 2,47
→ C2H4 và C3H6.
• Đặt nC2H4 = a mol; nC3H6 = b mol.