Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

BTKL có: nO trong Y = (3,24 - 0,04.56 - 0,015.64)/16 = 0.0025 mol


Đáp án B

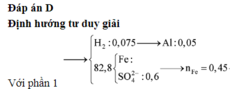
Xét phần 1: do sinh ra H2 ⇒ Al dư. nH2 = 0,075 mol ⇒ nAl dư = 0,05 mol.
Rắn không tan là Fe. Ta có: 2H2SO4 + 2e → SO2 + SO42– + 2H2O.
⇒ nSO42– = nSO2 = 0,6 mol ⇒ nFe = (82,8 – 0,6 × 96) ÷ 56 = 0,45 mol.
8Al + 3Fe3O4 → 4Al2O3 + 9Fe ⇒ nAl2O3 = 0,45 × 4 ÷ 9 = 0,2 mol.
⇒ mphần 1 = 0,05 × 27 + 0,2 × 102 + 0,45 × 56 = 46,95(g) ⇒ m phần 2 = 187,8(g).
⇒ phần 2 gấp 4 lần phần 1 ⇒ phần 2 chứa 0,2 mol Al; 0,8 mol Al2O3; 1,8 mol Fe.
Ta có: nH+ = 4nNO + 2nNO2 + 2nO + 10nNH4+ ⇒ nNH4+ = 0,015 mol.
Đặt nFe(NO3)2 = b ⇒ a + b = nFe = 1,8 mol; Bảo toàn electron:
0,2 × 3 + 3a + 2b = 1,25 × 3 + 1,51 + 0,015 × 8. Giải hệ có: a = 1,18.
Đáp án D

Giải thích:
Phần 1:
nH2 = 0,075 => nAldư = 0,05
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
8x→ 3x →4x → 9x
Chất rắn không tan trong NaOH là Fe (9x mol). Với H2SO4 đặc nóng
=> Fe3+ (u) và Fe2+ (v)
Bảo toàn electron: 3u + 2v = 0,6 . 2
m muối = 400a/2 + 152b = 82,8
=> u = 0,3 và v = 0,15
=> 9x = u + v => x = 0,05
Vậy phần 1 chứa Al (0,05), Al2O3 (0,2) và Fe (0,45)
=> mPhần 1 = 46,95
=> mPhần 2 = mX - mPhần 1 = 187,8
=> mPhần 2 = 4mPhần 1
Vậy phần 2 chứa các chất có số mol gấp 4 phần 1.
Phần 2 chứa Al (0,2), Al2O3 (0,8) và Fe (1,8)
=> nO = 0,8 . 3 = 2,4
nH+ = 12,97 = 4nNO + 2nNO2 + 2nO + 10nNH4+
=> nNH4+ = 0,015
Dung dịch A chứa Fe3+ (a mol), Fe2+ (y mol) và các ion khác.
Bảo toàn Fe => a + b = 1,8
Bảo toàn electron => 3a + 2b + 0,2 . 3 = 1,25 . 3 + 1,51 + 0,015 . 8
=> a = 1,18 và b = 0,62
Đáp án D

Đáp án A
m X = 136a => m O = 11,36 => n O = 0,71 mol
Quy đổi hỗn hợp X về a mol Mg, 2a mol Fe và 0,71 mol O.
Y tác dụng với HNO3 dư tạo ra khí NO, N2O và dung dịch chứa muối NH4NO3.
Cô cạn dung dịch thu được rắn chứa a mol Mg(NO3)2 , 2a mol Fe(NO3)3 và NH4NO3.
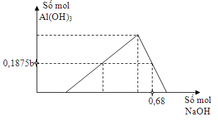
→ n N H 4 N O 3 = 0 , 1875 a
Do vậy số mol NO và N2O đều là 0,1875a.
Bảo toàn e: 2a + 2a.3 = 0,71.2 + 0,1875a.3 + 0,1875a.8 + 0,1875a.8
Giải được: a=0,32.
Đốt hỗn hợp X bắng Cl2 và O2 thu được Z.
Hòa tan Z cần 1,6 mol HCl → n O = 0 , 8 → n O 2 = 0 , 4
Gọi số mol Cl2 là x , kết tủa thu được là AgCl 2x +1,6 và Ag.
Bảo toàn e: n A g = 0,32.2 + 0,64.3 - 0,8.2 - 2x = 0,06 - 2x
=> 108(0,96 - 2x) + (108 + 35,5)(2x + 16) = 354,8
Giải được: x=0,3.
=> V = (0,3 + 0,4).22,4 = 15,68
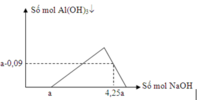
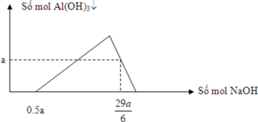
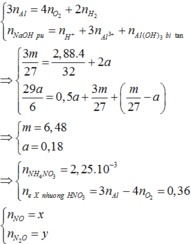


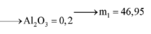
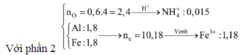
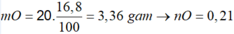
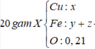
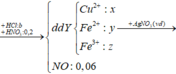
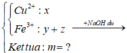
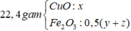
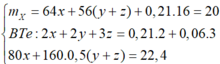
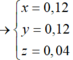
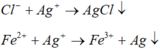
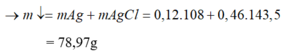
Đáp án A
Định hướng tư duy giải