Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích:
Do tỉ khối hơi của X so với O2 không đổi với mọi tỉ lệ mol của 2 este nên 2 este là đồng phân của nhau.
MX = 136 => C8H8O2
Do X tác dụng với NaOH sau phản ứng thu được hai muối khan nên 2 este trong X là:
HCOOCH2C6H5 (x mol) và HCOOC6H4CH3 (y mol)
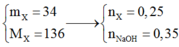
x+y = nX = 34/136 = 0,25
x + 2y = nNaOH = 0,35
=> x = 0,15; y = 0,1
Muối gồm HCOONa (0,25 mol) và CH3C6H4ONa (0,1 mol)
=> Phần trăm từng muối là 56,67% và 43,33%
Đáp án C

Đáp án B
● Giả sử không có este của phenol
⇒ nH = nNaOH = nhh Ancol = 0,46 mol.
+ Bảo toàn khối lượng
⇒ nhh Ancol = mH + mNaOH – mMuối = 12,72 gam.
⇒ MTrung bình ancol = ![]() = 27,65
= 27,65
⇒ Vô lý vì ancol bé nhất là CH3OH (32).
⇒ Có este của phenol.
+ Giải hỗn hợp T ta có:
Từ tỉ khối hơi ⇒ 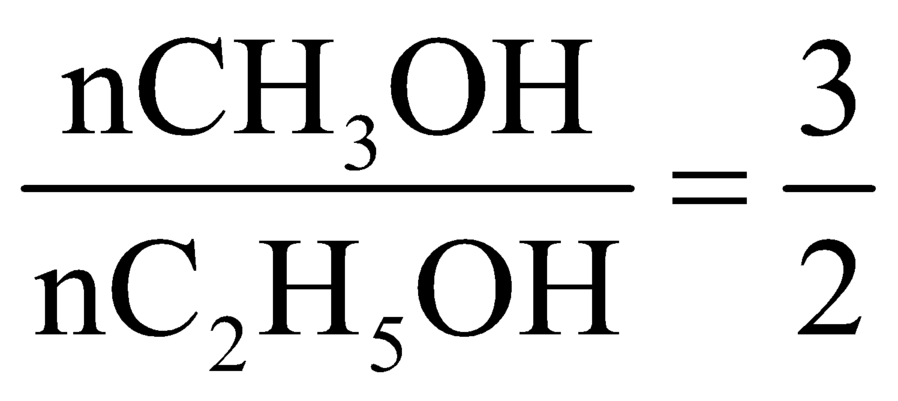
⇒ Đặt nCH3OH = 3a và nC2H5OH) = 2a.
+ Vì có muối của phenol
⇒ Có tạo ra H2O ⇒ Đặt nH2O = b.
⇒ 32×3a + 46×2a + 18b = 12,72
⇔ 156a + 18b = 12,72 (1).
⇒ 3a + 2a + 2b = nNaOH
⇔ 5a + 2b = 0,46 mol (2).
+ Giải hệ (1) và (2) ⇒ a = 0,06 và b = 0,08 mol
⇒ nhh este = 0,46 – 0,08 = 0,36 mol.
+ Bảo toàn oxi
⇒ nO/CO2 = 0,38×2 + 2,22×2 – 1,12 = 4,08
⇒ nCO2 = 2,04 mol
● Giải theo kinh nghiệm: X và Y sẽ cho cùng 1 muối và riêng Z sẽ tạo 2 muối.
+ Gọi số cacbon trong X, Y và Z lần lượt là a b và c
⇒ PT theo số mol CO2:
0,18a + 0,12b + 0,08c = 2,04.
⇒ Giải PT nghiệm nguyên ta có: a = 4, b = 5 và c = 9.
+ Gọi số nguyên tử hiđro trong X Y và Z lần lượt là a b và c
⇒ PT theo số mol H: 0,18a + 0,12b + 0,08c = 2,24.
⇒ Giải Pt nghiệm nguyên ta có: a = 4, b = 6 và c = 10.
● Vậy hỗn hợp H chứa
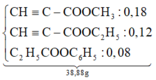
⇒ %mY = 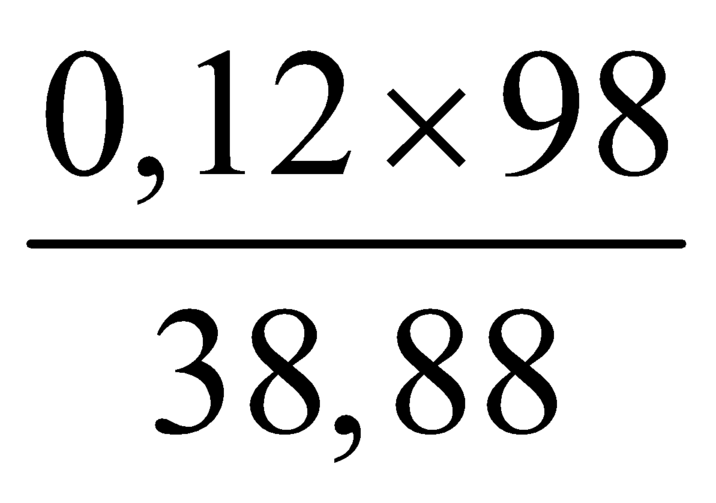 ≈ 30,35%
≈ 30,35%

Chọn D.
Hỗn hợp E gồm X, Y (este đơn chức, mạch hở): a mol và Z (este của phenol): b mol
Khi cho E tác dụng với NaOH thì: n N a O H = a + 2 b = 0 , 46 (1)
Hai ancol liên tiếp nhau có MT = 37,6 Þ CH3OH (3x mol) và C2H5OH (2x mol) Þ a = 5x (2)
→ B T K L m + 18 , 4 = m + 5 , 68 + m a n c o l + 18 b ⇒ 12 , 72 = 32 . 3 x + 2 x . 46 + 18 b (3)
Từ (1), (2), (3) suy ra x = 0,06 ; a = 0,3 ; b = 0,08
Xét phản ứng đốt cháy: 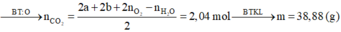
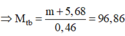 Þ Trong muối có thể có CH3COONa, C2H5COONa, CH2=CHCOONa CHºCCOONa.
Þ Trong muối có thể có CH3COONa, C2H5COONa, CH2=CHCOONa CHºCCOONa.
Trong 3 muối trên thì chỉ có CHºCCOONa thỏa mãn:
(kX,Y – 1).0,3 + (kZ – 1).0,08 = 0,92 (kZ = 5, kX,Y = 3)
Hỗn hợp E gồm CHºCCOOCH3; CHºCCOOC2H5; C2H5COOC6H5.
Vậy Y là CHºCCOOC2H5: 0,12 mol Þ %mY = 30,35%.

Đáp án là A
n N a O H : n K O H = 3 : 1 ⇒ Thay bằng kiềm chung MOH với M = 23 . 3 + 39 4 = 27
n A < n N a O H + n K O H ⇒ A chứ este của phenol
Tự chọn n A = 1 , gồm este của ancol ( u mol) và este của phenol (v mol)
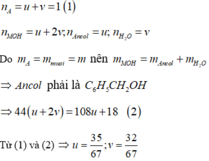
Y không tráng gương nên X là H C O O C H 2 - C 6 H 5 ( 35 / 67 )
=> Y là C H 3 C O O C 6 H 5 ( 32 / 67 )
=> %X= 52,24%

Chọn đáp án D
Vì tạo ra hỗn hợp ancol ⇒ hỗn hợp ancol chỉ có thể là CH3OH và C6H5CH2OH.
+ Đặt nH3OH = a và nC6H5CH2OH = b
⇒ Có hệ: 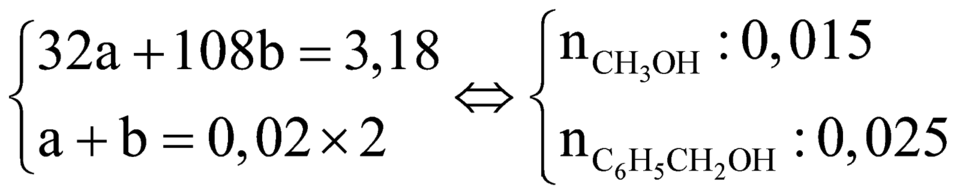
+ Vì nhỗn hợp este = 0,08 nhưng nHỗn hợp ancol = 0,04 ⇒ Có (0,08 – 0,04) = 0,04 mol
Este tạo chức phenol.
⇒ nH2O = 0,04 mol ⇒ nNaOH pứ = 0,04 + 0,04×2 = 0,12 mol.
+ Rõ ràng là bảo toàn khối lượng rồi. Tính m thôi.
mChất rắn = 10,88 + 6,72 – 3,18 – 0,72 = 13,7 gam
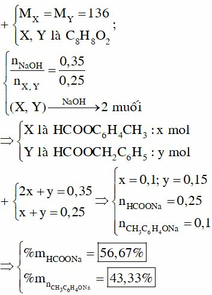

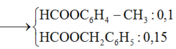
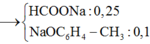
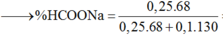
Đáp án D
► MX không đổi với mọi tỉ lệ mol của 2 este
⇒ 2 este có cùng M.
⇒ là đồng phân của nhau
MX = 136 (C8H8O2) ⇒ nX = 0,025 mol.
Do nKOH : nX = 0,035 : 0,025 = 1,4
⇒ chứa este của phenol.
► Đặt neste của ancol = x; neste của phenol = y
⇒ nX = x + y = 0,025 mol.
nKOH = x + 2y = 0,035 mol
⇒ giải hệ có: x = 0,015 mol; y = 0,01 mol.
Do Y gồm 2 muối ⇒ 2 este là HCOOCH2C6H5 và HCOOCH2C6H4CH3.
► Y gồm (0,015 + 0,01 = 0,025) mol HCOOK và 0,01 mol CH3C6H4OK.
||⇒ m = 0,025 × 84 + 0,01 × 146 = 3,56(g)