Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
→ n O 2 ( C H 3 O H ) = 15 , 68 22 , 4 - 20 32 = 0 , 075
→ n C H 3 O H = 0 , 05 → n Y = 0 , 05
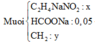
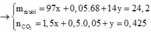
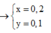
n G l y > n A l a → n A l a ∈ ( 0 ; 0 , 1 )
→ C H 3 C O O N a
→ n A l a = 0 , 05 → n G l y = 0 , 15
→ n G l y : n A l a = 3 : 1

Chọn đáp án C
Nhận xét: X + NaOH → Muối + H2O || Y + NaOH → Muối + CH3OH.
Do NaOH và H2O không đốt được ⇒ độ chênh lệch mol O2 là do đốt CH3OH.
||⇒ nY = nCH3OH = ∆nO2 ÷ 1,5 = (0,7 – 0,625) ÷ 1,5 = 0,05 mol.
► Quy E về C2H3NO, CH2, H2O và HCOOCH3 ⇒ nHCOOCH3 = 0,05 mol.
Đặt nC2H3NO = x; nCH2 = y ⇒ nO2 đốt E = 2,25x + 1,5y + 0,05 × 2 = 0,7 mol.
● Muối gồm x mol C2H4NO2Na; y mol CH2 và 0,05 mol HCOONa.
mmuối = 97x + 14y + 0,05 × 68 = 24,2(g) || Giải hệ có: x = 0,2 mol; y = 0,1 mol.
Do nGly-Na > nAla-Na ⇒ ghép 1 CH2 vào HCOONa ⇒ dư 0,05 mol CH2.
⇒ nAla = nCH2 còn = 0,05 mol ⇒ nGly = 0,2 - 0,05 = 0,15 mol.
► Gly : Ala = 0,15 ÷ 0,05 = 3 : 1 ⇒ chọn C.

Đáp án C
n O2 đốt cháy E = 0,7 mol
n O2 đốt cháy muối = 0,625 mol
n O2 chênh lệch chính là phần dùng để đốt cháy CH3OH do phản ứng thủy phân sinh ra
CH3OH + 1,5 O2→ CO2 + 2 H2O
0,05 0,075
Đặt công thức chung của muối amino axit là CnH2nO2NNa
Và muối của axit là CmH2m-1O2Na
2 CnH2nO2NNa + ( 3n – 1,5 ) O2→ ( 2n – 1 ) CO2 + 2 n H2O + Na2CO3 + N2
2 CmH2m-1O2NNa + ( 3 m – 2 ) O2→ ( 2 m – 1 ) CO2 + ( 2m -1 ) H2O + Na2CO3
Theo PTHH : n O2 = a . ( 3n – 1,5 ) : 2 + b . ( 3m – 1 ) : 2 = 0,625 mol
=> 3 ( na+ mb ) - 1,5 a – 2b = 1,25
n CO2 = a . ( 2n – 1 ) : 2 + b . ( 2m – 1 ) :2 = 0,425
=> 2 ( na + mb ) – a – b = 0,85
m muối = a ( 14n + 69 ) + b ( 14m + 54 ) = 24,2
=> 14 ( na + mb ) + 69 a + 54 b = 24,2
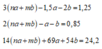
=> na + mb = 0,55 và a = 0,2 b = 0,05
na + m b = 0,55 => n . 0,2 + m . 0,05 = 0,55 => 4 n + m = 11
Vì 3 >n > 2 ( n là giá trị trung bình của 2 muối gly và ala )
1 ⩽m => m = 1 ; n = 2,5 => n Gly : n Ala = 1 : 1 ( 2,5 nằm giữa 2 và 3 )
hoặc m = 2 thì n = 2,25 =>n Gly : n Ala = ( 3- 2,25 ) : (2,25 – 2 ) = 3: 1 ( dùng phương pháp đường chéo )

n O 2 đ ố t c h á y E = 0 , 7 m o l n O 2 đ ố t c h á y m u ố i = 0 , 625 m o l
n O 2 chênh lệch chính là phần dùng để đốt cháy C H 3 O H do phản ứng thủy phân sinh ra
C H 3 O H + 1 , 5 O 2 → C O 2 + 2 H 2 O
0,05 0,075
Đặt công thức chung của muối amino axit là C n H 2 n O 2 N N a
Và muối của axit là C m H 2 m − 1 O 2 N a
2 C n H 2 n O 2 N N a + 3 n – 1 , 5 O 2 → 2 n – 1 C O 2 + 2 n H 2 O + N a 2 C O 3 + N 2 2 C m H 2 m − 1 O 2 N N a + 3 m – 2 O 2 → 2 m – 1 C O 2 + 2 m – 1 H 2 O + N a 2 C O 3
Theo PTHH : n O 2 = a . 3 n – 1 , 5 : 2 + b . 3 m – 1 : 2 = 0 , 625 m o l
=> 3 (na+ mb) – 1,5 a – 2b = 1,25
n C O 2 = a . 2 n – 1 : 2 + b . 2 m – 1 : 2 = 0 , 425
=> 2 (na + mb) – a – b = 0,85
m m u ố i = a ( 14 n + 69 ) + b ( 14 m + 54 ) = 24 , 2
=> 14 (na + mb) + 69 a + 54 b = 24,2
3 n a + m b − 1 , 5 a − 2 b = 1 , 252 n a + m b − a − b = 0 , 8514 n a + m b + 69 a + 54 b = 24 , 2
=> na + mb = 0,55 và a = 0,2 b = 0,05
na + m b = 0,55 => n . 0,2 + m . 0,05 = 0,55 => 4 n + m = 11
Vì 3 >n > 2 ( n là giá trị trung bình của 2 muối gly và ala )
1 ≤ m = > m = 1 n = 2 , 5 = > n G l y : n A l a = 1 : 1 (2,5 nằm giữa 2 và 3)
hoặc m = 2 t h ì n = 2 , 25 = > n G l y : n A l a = 3 − 2 , 25 : 2 , 25 – 2 = 3 : 1 (dùng phương pháp đường chéo )
Đáp án cần chọn là: C

Chọn đáp án C
Nhận xét: X + NaOH → Muối + H2O || Y + NaOH → Muối + CH3OH.
Do NaOH và H2O không đốt được ⇒ độ chênh lệch mol O2 là do đốt CH3OH.
||⇒ nY = nCH3OH = ∆nO2 ÷ 1,5 = (0,7 – 0,625) ÷ 1,5 = 0,05 mol.
► Quy E về C2H3NO, CH2, H2O và HCOOCH3 ⇒ nHCOOCH3 = 0,05 mol.
Đặt nC2H3NO = x; nCH2 = y ⇒ nO2 đốt E = 2,25x + 1,5y + 0,05 × 2 = 0,7 mol.
● Muối gồm x mol C2H4NO2Na; y mol CH2 và 0,05 mol HCOONa.
mmuối = 97x + 14y + 0,05 × 68 = 24,2(g) || Giải hệ có: x = 0,2 mol; y = 0,1 mol.
Do nGly-Na > nAla-Na ⇒ ghép 1 CH2 vào HCOONa ⇒ dư 0,05 mol CH2.
⇒ nAla = nCH2 còn = 0,05 mol ⇒ nGly = 0,2 - 0,05 = 0,15 mol.
► Gly : Ala = 0,15 ÷ 0,05 = 3 : 1 ⇒ chọn C.

Đáp án C
Qui hỗn hợp E về E2: x mol đipeptit (Gly,Ala) và y mol Este
Ta thấy NaOH và H2O không cần O2 để đốt; CH3OH cần 1,5y mol O2 để đốt
⇒ Bảo toàn O có: 0,7 = 0,625 + 1,5y ⇒ y = 0,05 mol
Mặt khác, hỗn hợp qui đổi E2 đốt cháy cho số mol:
nCO2 = nH2O = (3x + 2y + 0,7.2).3 = (x + 0,5) mol
mE2=14.(0,5 + x ) + 76x + 32y (g)
Mà nNaOH dùng = (2x + 0,05) mol
Bảo toàn khối lượng :
14.(0,5 + x) + 76x + 32y + 40.(2x + 0,05) = 24,2 + 18x + 32y
⇒ x = 0,1 mol
⇒ Có C trung bình trong E2 = 0,6/(0,1 + 0,05) = 4
⇒ Số Ceste ≤ 3. Có 2 trường hợp xảy ra:
TH1: este là HCOOCH3. Gọi số mol Gly = a; Ala = b thì có:
⇒ 2a + 3b = 0,6 – 0,05.2 và a + b = 0,2
⇒ a = b = 0,1 mol (Loại do nGly > nAla)
TH2: este là CH3COOCH3
⇒ 2a + 3b = 0,45 và a + b = 0,2
⇒ a = 0,15; b = 0,05 (TM)
Thủy phân X trong HCl thu được ClH3NCH2COOH : 0,15 mol và 0,05 mol ClH3NC2H4COOH
→ tỉ lệ khối lượng = 2,67
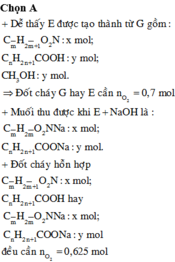


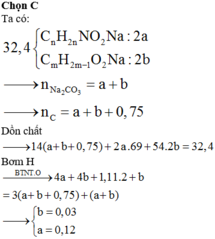
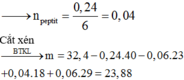
Chọn A