Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D

Dung dịch Y gồm Fe3+ (0,122), SO42- (0,004), H+ (0,034), NO3- ( → BTDT 0,392)
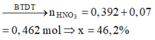

Đáp án A
mC = 90.6,667/100 = 6 (g)
=> nC = 0,5 mol
mFe = 84 (g) => nFe = 1,5 mol
Fe + 6HNO3 → Fe(NO3)3 + 3NO2 + 3H2O
nFe= 1,5 => nNO2=4,5 mol
C + 4HNO3 → 4NO2 + CO2 + 2H2O
nC=nCO2=0,5 mol
n khí = nNO2 + nCO2 = 4,5 + 0,5 = 5 mol
=> V = 112 lít

+ Tính được những gì có thể tính được
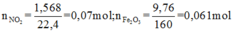
+ Với bài toán gồm nhiều giai đoạn liên tiếp nhau như thế này ta nên tóm tắt lại bài toán:
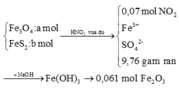
Bây giờ ta phải thiết lập được mối quan hệ giữa a và b với hi vọng là tìm được a và b rồi sau đó áp dụng các định luật bảo toàn như khối lượng, nguyên tố, electron ....
+ Bảo toàn nguyên tố Fe: 3a + b = nFe = 2.0,061 = 0,122
+ Bảo toàn sốmol electron trao đổi: a + 15b = 0,07.1 ( Chú ý FeS2→Fe3+ + 2S+6 + 15e)
Giải được a = 0,04; b = 0,002.
+ Tiếp tục sử dụng bảo toàn nguyên tố S:
![]()
+ Vì phản ứng xảy ra hoàn toàn và vừa đủ nên sau khi phản ứng với dung dịch NaOH ta chỉ thu được 2 muối là Na2SO4 và NaNO3.
Áp dụng định luật bảo toàn nguyên tố Na:
![]()
+ Cuối cùng dựa vào sơ đồ tóm tắt, ta sẽ dùng bảo toàn nguyên tố N
![]()
=>![]()
Đáp án D

Đáp án B
Định hướng tư duy giải
Nhận thấy, nếu Z chỉ là H2 sẽ vô lý ngay vì
không có sản phẩm khử nào thỏa mãn.
→ Khí thoát ra ở cả hai lần phải là hỗn hợp khí NH3 và H2.
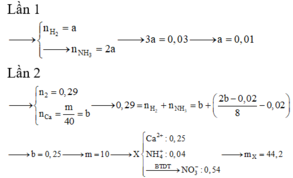

Đáp án C
nHNO3 bđ = 1,5 ; nNO2 = 0,2 (mol)
Khi thêm nước lọc vào T và thu được lượng kết tủa max thì phần dung dịch nước lọc chỉ chứa NaNO3.
Bảo toàn N => nNaNO3 = nHNO3 – nNO2 = 1,3 (mol)
=> nNaOH = 1,3 => Vdd NaOH = 1,3 (lít)
Đặt a, b là số mol Fe3O4 và CuO
mhh = 232a + 80b = 29,2 (1)
Có: nCO2 = nBaCO3 = 0,05 (mol) = nO( trong oxit pư)
Bảo toàn e cả quá trình: nNO2 = nFe3O4 + 2nO (mất đi khi + CO)
=> nFe3O4 = nNO2 - 2nO (mất đi khi + CO) = 0,2 – 2.0,05 = 0,1 (mol)
=> %mFe3O4 = [0,1. 232: 29,2].100% = 79,45%


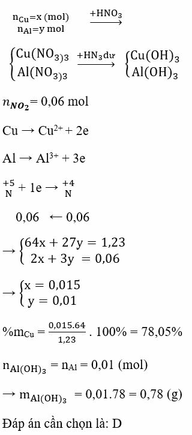
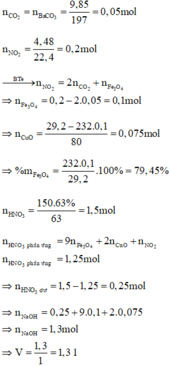
Fe+6HNO3- -->Fe(NO3)3 + 3NO2 + 3H2O
x 6x 3x
mdds=mddt+mFe-mNO2
(126-63*6x)=0.3692*(200+56x-3x*46)
=>x==0.15=>nNO2=0.45=>V=nRT/p=9.89l
nHNO3 = 63%x200/63 = 2 mol
Do acid dư nên Fe --> Fe3+
Gọi m là khối lượng Fe: --> nFe = m/56
2H+ + NO3- + 1 e --> NO2 + H2O
số mol e nhường = số e nhận
--> 3m/56 = nNO2
--> Cứ 2 mol acid tham gia phản ứng thì có 1 mol NO3- của acid tham gia tạo muối và 1 mol tạo khí NO2.
--> lượng acid phản ứng là 3m/56 x 2 = 3m/28
--> (2 - 3m/28)x63/( m+ 200 - 46x3m/56) = 0.3692
-->m = 8.4
--> số mol NO2 là 0.45
n = pV/RT = 1,12xV/0.082x(27+273) = 0.45 --> V = 9.8839(l)\(\approx\)9,89 (l)