Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
• Sục từ từ đến dư khí CO2 vào dung dịch X thì thấy xuất hiện kết tủa là Al(OH)3.
=> X chứa AlO 2 - ⇒ n Ba > 3 2 n Al 3 +
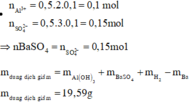
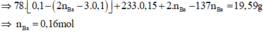
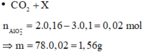
Gần nhất với giá trị 1,6

Đáp án B
Xét NaOH +X
tạo 0,52 mol NaCl và 0,14 mol N a 2 S O 4 và dư 0,05 mol N a +
Ghép với A l O 2 - ⇒ tạo 0,05 mol N a A l O 2
Đặt n A l = x ; n M g = y
![]()
![]()
Giải hệ có: ![]()
![]()
TH1: B a S O 4 đạt cực đại
⇒ n B a ( O H ) 2 = n S O 4 = 0 , 14 m o l
⇒ n K O H = 0 , 14 . 8 = 1 , 12 m o l
Ghép tương tự NaOH, ta thấy B a 2 + , K + , S O 4 2 - , C l - còn dư 0,6 mol điện tích
Ghép với A l O 2 - ⇒ ghép được 0,15 mol
⇒ vẫn chưa đủ ⇒ còn O H - dư
Rắn gồm 0,14 mol B a S O 4 ; 0 , 15 m o l M g O ⇒ mrắn =38,62g
TH2: A l ( O H ) 3 đạt cực đại
⇒ các ion trong dung dịch gồm B a 2 + , K + , S O 4 2 - , C l -
(ta đang giả sử B a 2 + , S O 4 2 - cùng tồn tại trong cùng 1 dung dịch)
Đặt n B a 2 + = a ⇒ n K + = 8 a
Bảo toàn điện tích:
![]()
n B a S O 4 = n B a 2 + = 0 , 08 m o l
![]()
![]()
⇒ mrắn tối đa =38,62 (g)

Đáp án B
• ![]()
• Đặt số mol Mg, Al lần lượt là a, b => 24a + 27b = 7,65 g (1)
Có n NaOH = 0 , 85 > 0 , 52 + 2 . 0 , 14 = 0 , 8
=> Chứng tỏ Al(OH)3 bị hòa tan một phần: n AlO 2 - = 0 , 85 - 0 , 8 = 0 , 05 mol
⇒ m ↓ = m Mg ( OH ) 2 + m Al ( OH ) 3 = 58 a + 78 . ( b - 0 , 05 ) = 16 , 5 g (2)
• Từ (1) và (2) suy ra a = b = 0,15
• Đặt V (lít) là thể tích dung dịch kiềm thêm vào.
⇒ n B a 2 + = 0 , 1 V , n OH - = ( 0 , 8 + 2 . 0 , 1 ) V = V
P Lượng hiđroxit thu được cực đại khi: n OH - = n H + ⇒ V = 0 , 8 ( l )
Khi đó: n B a 2 + = 0 , 08 mol < n SO 4 2 - = 0 , 14 mol
⇒ m ↓ = 58 . 0 , 15 + 78 . 0 , 15 + 233 . 0 , 08 = 39 , 04 g
P Lượng BaSO4 thu được cực đại khi: n Ba 2 + = n SO 2 - = 0 , 14 mol ⇒ n OH - = 1 , 4 mol
Khi đó: n OH - > n H + + n Al ⇒ Al ( OH ) 3 tan hết
⇒ m ↓ = 58 . 0 , 15 + 233 . 0 , 14 = 41 , 32 g > 39 , 04 g
=> Lượng kết tủa đạt cực đại khi V = 1,4 lít
⇒ m ↓ = m MgO + m B a S O 4 = 40 . 0 , 15 + 233 . 0 , 14 = 38 , 62 g
Gần nhất với giá trị 38,6

Đáp án A
Khi thêm 0,85 mol NaOH vào X thì thu được dung dịch chứa NaCl: 0,52 mol và Na2SO4 : 0,14mol;
Vì n N a O H > n N a C l + 2 n N a 2 S O 4 nên còn N a A l O 2
Bảo toàn Na có n N a O H = n N a C l + 2 n N a 2 S O 4 + n N a A l O 2 → 0 , 85 = 0 , 52 + 2 . 0 , 14 + n N a A l O 2
→ n N a A l O 2 = 0,05 mol
Kết tủa thu được là M g ( O H ) 2 : x mol và A l ( O H ) 3 : y mol
Ta có hệ sau
→ dd X có A l + 3 : 0 , 15 m o l ; M g + 2 : 0 , 15 m o l ; C l - : 0 , 52 m o l ; S O 4 2 - : 0 , 14 m o l
Ta thấy X có 3 n A l + 2 n M g < n C l + 2 n S O 4 nên X có dư H + → n H + = 0,52 + 0,14.2 -0,15.3 -0,15.2 = 0,05 mol
OH- + H + → H2O
OH- + M g + 2 → M g ( O H ) 2
3OH- + A l + 3 → A l ( O H ) 3
B a 2 + + S O 4 2 - → B a S O 4
A l ( O H ) 3 + O H - → A l O 2 - + 2 H 2 O
Khi thêm 8x mol KOH và x mol B a ( O H ) 2 vào dung dịch X thì để thu được lượng kết tủa lớn nhất ta xét các TH sau
TH1 : kết tủa có B a S O 4 : 0,14 mol và M g ( O H ) 2 : 0,15 mol và có thể có A l ( O H ) 3
Bảo toàn Ba có x = 0,14 mol → n O H =8x + 2x =10x =1,4 mol > 2 n M g + 4 n A l + n H + = 0,95
→ phản ứng có kết tủa A l ( O H ) 3 bị hòa tan hết → kết tủa thu được là B a S O 4 và M g ( O H ) 2
→ đem nung thu được B a S O 4 : 0,14 mol và MgO : 0,15 mol → m = 38,62g
TH2: Kết tủa có A l ( O H ) 3 : 0,15 mol và Mg(OH)2: 0,15 mol; B a S O 4
Ta có n O H = 10x = 0,15.3 + 0,15.2 +0,05=0,8 → x = 0,08 mol→ có 0,08 mol B a S O 4
→ Đem nhiệt phân thu được 0,08 mol B a S O 4 ; 0,075 mol Al2O3 và 0,15mol MgO
→ m = 0,08.233 + 0,075.102 +0,15.40 =32,29g
Nên TH1 khối lượng kết tủa lớn nhất là 38,62 g gần nhất với 38,6 nhất

Đáp án C
· Phần 1 qua Ca(OH)2 dư:
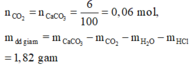
![]() Không khí bị hấp thụ là N2:
Không khí bị hấp thụ là N2:
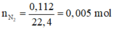
·Phần 2: Kết tủa thu được là AgCl
![]()
![]()
![]()
Vì
![]()
trong phần 1 có
![]()
Vậy khi đốt cháy 5,52 gam X tạo ra 0,18 mol CO2; 0,135 mol H2O; 0,015 mol N2; 0,06 mol HCl
· Áp dụng định luật bảo toàn khối lượng có:
= 44.0,18 + 18.0,135 + 28.0,015 + 36,5.0,06 – 5,52 = 7,44 gam
![]()
· Áp dụng định luật bảo toàn nguyên tố O có:
nO(X) = 2.0,18 + 0,135 – 2.0,2325 = 0,03 mol

X có công thức C6H11ONCl2. Vậy MX = 184

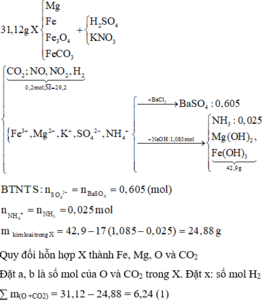

Từ (1), (2) và (3)
=> a = 0,28 (mol) ; b = 0,04 (mol) ; x = 0,06 (mol
=> m = 24,88 + 39 ( 0,255 –b –x) + 0,025.18 + 0,605.96 = 88, 285 => nhận định a) sai
nKNO3 = 0,225 – b – x = 0,125 => nhận định b) sai
%FeCO3 = ( 0,04.116/ 31,12).100% = 14,91% => nhận định c) sai
nO = 4nFe3O4 + nFeCO3 => nFe3O4 = 0,06 => nhận định d) sai
=> có tất cả 4 nhận định sai.

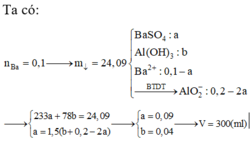

Đáp án B
Ta có : n A l 2 ( S O 4 ) 3 = 0 , 5 m o l
Cho Ba tác dụng với Al2(SO4)3 tức là cho Ba tác dụng với H2O tạo ra Ba(OH)2 sau đó chất này tan.
Gọi số mol Ba là x. Ta có số mol kết tủa BaSO4 tạo ra là 0,15, số mol H2 là x mol.
Ta có: n A l ( O H ) 3 = 4 n A l 3 + - n O H - = 0 , 1 . 4 - 2 x
Áp dụng bảo toàn khối lượng, khối lượng dung dịch giảm là:
Giải được: x = 0,16.
→ n A l O 2 - = 0 , 1 - ( 0 , 4 - 2 x ) = 0 , 02 m o l
Vậy khi sục CO2 dư vào X thì kết tủa tạo ra là Al(OH)3 0,02 mol (không thể có BaCO3).
→ m = 1 , 56 g a m