Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Gọi
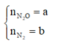
Có
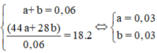
Ta có nAl = 0,46 Þ ne nhường = 3nAl = 1,38mol
Nếu sản phẩm khử có NH4NO3 thì
![]()
Do đó sản phẩm khử có chứa NH4NO3
Áp dụng định luật bảo toàn mol electron, ta có:
n e n h ư ờ n g = n e n h ậ n
![]()

Khi đó
![]()
Chú ý: Đề bài cho đồng thời các dữ kiện để có thể tính được số mol nhôm và số mol các sản phẩm khử là các khí, trong khi để tính được lượng muối nitrat của kim loại thì chỉ cần một trong hai dữ kiện trên.
Khi đó đề bài có vẻ "thừa". Tuy nhiên những bài như vậy thường có sự tạo thành muối amoni nền các bạn cần kiểm tra có sự tạo thành muối này không thông qua việc so sánh giữa số mol electron cho và số mol electron nhận.

Câu 1 :\(n_{CO_2} = \dfrac{2,688}{22,4} = 0,12(mol)\)
MgCO3 + 2HCl \(\to\) MgCl2 + CO2 + H2O
..................................0,12........0,12..................(mol)
Suy ra: a = 0,12.95 = 11,4(gam)
Câu 2 :
\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ \Rightarrow n_{Cu} = 2n_{Fe} = 0,15.2 = 0,3(mol)\\ 2Fe+3Cl_2\xrightarrow{t^o} 2FeCl_3\\ Cu+Cl_2 \xrightarrow{t^o} CuCl_2\\ n_{Cl_2} = \dfrac{3}{2}n_{Fe} + n_{Cu} = 0,525\\ \Rightarrow V = 0,525.22,4 =11,76(lít)\)

\(a,n_{H_2}=\dfrac{2,576}{22,4}=0,115\left(mol\right)\\ Đặt:n_{Mg}=a\left(mol\right);n_{Al}=b\left(mol\right)\left(a,b>0\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ \Rightarrow\left\{{}\begin{matrix}95a+133,5b=10,475\\a+1,5b=0,115\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,04\\b=0,05\end{matrix}\right.\\ \%m_{Mg}=\dfrac{0,04.24}{0,04.24+0,05.27}.100\approx41,558\%\Rightarrow\%m_{Al}\approx58,442\%\\ b,n_{HCl}=2.n_{H_2}=2.0,115=0,23\left(mol\right)\\ \Rightarrow x=C\%_{ddHCl}=\dfrac{0,23.36,5}{100}.100=8,395\%\)

Đáp án D
Các phương trình phản ứng :
Phương trình phản ứng :
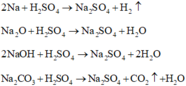
Hỗn hợp khí H2 và CO2
Dung dịch Y chỉ có Na2SO4 =>muối thu được khi cô cạn dung dịch Y là Na2SO4
Tinh toán:
Muối thu được là Na2SO4

Sơ đồ phản ứng :
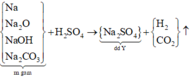
Bảo toàn gốc SO4 ta có :
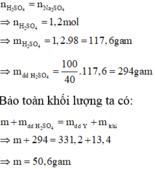

\(19,1gam\) \(:\left\{{}\begin{matrix}Al\\Mg\\Zn\end{matrix}\right.\)\(\underrightarrow{+O_2}\)\(Y:25,5gam\)\(\underrightarrow{+HCl}\left\{{}\begin{matrix}AgCl_3\\MgCl_2\\ZnCl_2\end{matrix}\right.\) + H2 : 0,3 mol
H2O
Áp dụng định luật bảo toàn khối lượng:
\(mO_2=25,5-19,1=6,4gam\) \(\Rightarrow nO_2=0,2\left(mol\right)\)
BTNT O : nH2O = 0,4mol
\(\rightarrow nHCl^-\left(tdOxi\right)=0,8\left(mol\right)\)
\(nH_2=0,3\left(mol\right)\rightarrow nCl^-\left(tdKl\right)=0,6\left(mol\right)\)
\(m_{muối}=19,1+\left(0,8+0,6\right).35,5=68,8\left(g\right)\)


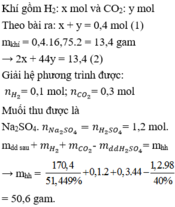
Gọi \(\left\{{}\begin{matrix}n_{H_2}=a\left(mol\right)\\n_{CO_2}=b\left(mol\right)\end{matrix}\right.\) => \(a+b=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
=> \(\overline{M}_X=\dfrac{2a+44b}{a+b}=2.6,25=12,5\left(g/mol\right)\)
=> a = 0,3; b = 0,1
PTHH: Fe + 2HCl --> FeCl2 + H2
0,3<--0,6<------0,3<---0,3
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
0,1<----0,2<------0,1<----0,1
CuO + 2HCl --> CuCl2 + H2O
x--->2x------->x
mrắn (sau pư) = 0,3.127 + 0,1.111 + 135x = 62,7
=> x = 0,1 (mol)
mA = 0,1.80 + 0,3.56 + 0,1.100 = 34,8 (g)
mHCl = (0,6 + 0,2 + 0,2).36,5 = 36,5 (g)
=> \(m'=\dfrac{36,5.100}{14,6}=250\left(g\right)\)