Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.Mg+HCl\rightarrow MgCl_2+H_2\\ b.n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\\ n_{MgCl_2}=n_{Mg}=0,1\left(mol\right)\\ \Rightarrow m_{MgCl_2}=0,1.95=9,5\left(g\right)\\ c.n_{H_2}=n_{Mg}=0,1\left(mol\right)\\ \Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)

a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)

Nzn=0,1mol
a) có pt : Zn + 2Hcl -> ZnCl2 + H2
1 -> 2 -> 1 -> 1 mol
0,1-> 0,2 -> 0,1 -> o,1 mol
b) số Hcl đã dùng khi pứ là :
0,2 . 36,5= 7,3
-> số gam hcl dư là 10,95- 7,3=3,65(g)
c)mZnCl2=0,1 . 136=13,6g

a) Lập công thức hóa học của muối kẽm clorua: Z n C l 2
b) Khối lượng muối Z n C l 2 = 6,5 + 7,3 – 0,2 = 13,6 (gam)

a, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,2}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{15}\left(mol\right)\Rightarrow m_{Fe}=\dfrac{2}{15}.56=\dfrac{112}{15}\left(g\right)\)

\(n_{HCl}=0,2.2=0,4\left(mol\right)\\ a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.0,2........0,4.......0,2.......0,2\left(mol\right)\\ m=m_{Zn}=0,2.65=13\left(g\right)\\ c.m_{ZnCl_2}=136.0,2=27,2\left(g\right)\\ d.V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)

a)
Zn + 2HCl → ZnCl2 + H2
b) nZn = \(\dfrac{3,5}{65}\)=\(\dfrac{7}{130}\) mol
Theo tỉ lệ phản ứng => nH2 = nZn= \(\dfrac{7}{130}\)mol
<=> V H2 = \(\dfrac{7}{130}\).22,4 = 1,206 lít
c) nZnCl2 = nZn => mZnCl2 = \(\dfrac{7}{130}\).136= 7,32 gam
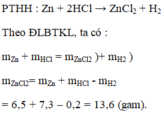
\(a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.n_{Zn}=\dfrac{65}{65}=1\left(mol\right)\\ n_{ZnCl_2}=n_{Zn}=1\left(mol\right)\\ \Rightarrow m_{ZnCl_2}=1.136=136\left(g\right)\\ c.n_{H_2}=n_{Zn}=1\left(mol\right)\\ \Rightarrow V_{H_2}=1.22,4=22,4\left(l\right)\)