Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nZn = nZn(NO3)2 = 0,66 mol ⇒ mZn(NO3)2 = 124,74 gam.
⇒ mNH4NO3 = 4,8 gam ⇒ nNH4NO3 = 0,06 mol.
+ Đặt số mol NO = a và nN2O = b ta có:
+ PT theo số mol hỗn hợp khí: a + b = 0,18 (1).
+ PT theo bảo toàn e: 3a + 8b + 0,06×8 = 0,66×2 (2).
+ Giải hệ (1) và (2) ta có nNO = 0,12 và nN2O = 0,08 mol.
⇒ ∑nHNO3 pứ = 0,12×4 + 0,06×10 + 0,06×10 = 1,68 mol.
⇒ mHNO3 = 105,84 gam ⇒ mDung dịch HNO3 = 1058,4 gam.
⇒ V = 1058,4 ÷ 1,26 = 840 ml.

Đáp án A
Số mol N2O = 1,008/22,4 = 0,045 mol;
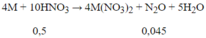
Số mol HNO3 phản ứng = 0,045.10 = 0,45 mol < 0,5 suy ra có tạo sản phẩm khử khác là NH4NO3
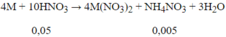
Vậy m = 8,9 + 62.( 8.0,045+8.0,005)+ 80.0.005=34,1g

Đáp án B
![]()
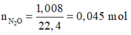
2NO−3 + 10H+ + 8e → N2O↑ + 5H2O
→ n N O 3 - ( m u ố i )
![]()
Ta thấy:
2 n N 2 O + n N O 3 - ( m u ố i ) = 0,045.2 + 0,36 = 0,45 mol < n H N O 3 =>Có muối NH4NO3.
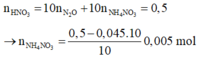
n N O 3 - ( m u ố i ) =
![]()
= 0,4 mol
![]()
![]()

Đáp án D
- Hướng tư duy 1: Bảo toàn nguyên tố N
- Quá trình:


![]()
+ Ta có
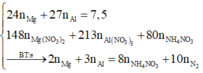
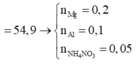
![]()
![]()
- Hướng tư duy 2: Tính theo số mol HNO3
+ Ta có
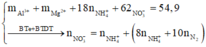
![]()
![]()

Đáp án D
![]()
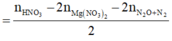
= 0,035
⇒ m m u ố i = 0 , 15 . 148 + 0 , 035 . 80 = 25 g a m


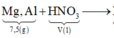
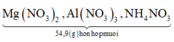
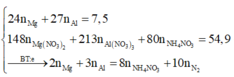
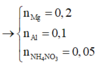

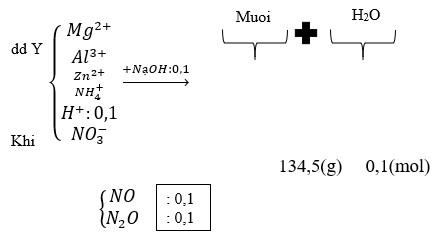

nZn = nZn(NO3)2 = 0,66 mol ⇒ mZn(NO3)2 = 124,74 gam.
⇒ mNH4NO3 = 4,8 gam ⇒ nNH4NO3 = 0,06 mol.
+ Đặt số mol NO = a và nN2O = b ta có:
+ PT theo số mol hỗn hợp khí: a + b = 0,18 (1).
+ PT theo bảo toàn e: 3a + 8b + 0,06×8 = 0,66×2 (2).
+ Giải hệ (1) và (2) ta có nNO = 0,12 và nN2O = 0,08 mol.
⇒ ∑nHNO3 pứ = 0,12×4 + 0,06×10 + 0,06×10 = 1,68 mol.
⇒ mHNO3 = 105,84 gam ⇒ mDung dịch HNO3 = 1058,4 gam.
⇒ V = 1058,4 ÷ 1,26 = 840 ml
Đáp án A