Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
M : x mol ; M2On : y mol
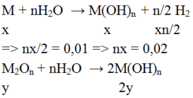
⇒ n M(OH)n = x + 2y = 0,02
+) n = 1 (KL kiềm ) ⇒ x = 0,02 ; y = 0 ⇒ loại
+) n = 2 (KL kiềm thổ) ⇒ x = 0,01 , y = 0,005
⇒ mhh = 0,01.M + 0,005.(2M + 16.2) = 2,9
⇒ M = Ba

Đáp án B
n H 2 SO 4 = 100 . 0 , 392 98 = 0 , 4 mol
Sau phản ứng thu được dung dịch Y chỉ chứa một chất tan Þ phản ứng vừa đủ, H2SO4 phản ứng hết
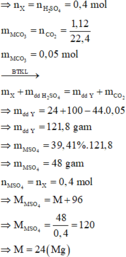

nếu HCl dư=> chỉ có 3 chất tan
Nếu HCl đủ=> chỉ có 2 chất tan
=> HCl thiếu => 2 muối và 2 dd kiềm
thay vào để giải nghiệm thì chỉ có Li và K thỏa mãn=> 2 kim loại cần tìm là Liti vs Kali

a) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: A + 2H2O --> A(OH)2 + H2
0,2<--------------0,2<-----0,2
=> \(M_A=\dfrac{8}{0,2}=40\left(g/mol\right)\)
=> A là Ca (Canxi)
b) \(C_M=\dfrac{0,2}{0,5}=0,4M\)

Đáp án A
Vì khối lượng hỗn hợp X sử dụng ở hai trường hợp là như nhau và hóa trị của các kim loại kiềm luôn là I không đổi nên số mol electron trao đổi ở hai trường hợp bằng nhau.
Áp dụng định luật bảo toàn mol electron ta có:
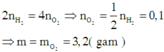

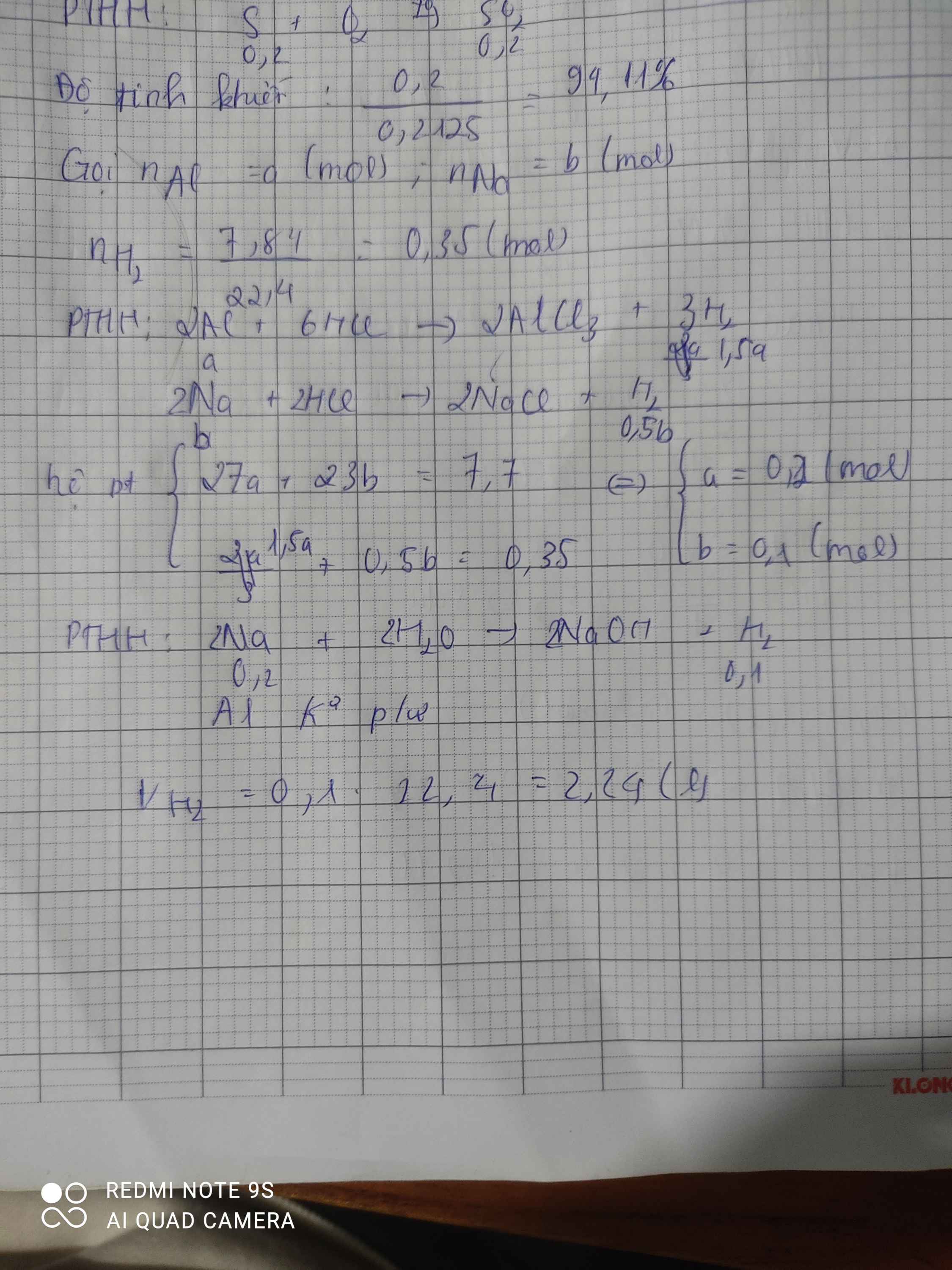
Đáp án C
M : x mol ; M2On : y mol
M + H2O → M(OH)n + n/2 H2
x x n 2 x
=> n 2 x = 0,01 => nx = 0,02
M2On + nH2O →2M(OH)n
y 2y
⇒ n M(OH)n = x + 2y = 0,02
+) n = 1 (KL kiềm ) ⇒x = 0,02 ; y = 0 ⇒ B. loại
+) n = 2 (KL kiềm thổ) ⇒ x = 0,01 , y = 0,05
⇒ mhh = 0,01.M + 0,05.(2M + 16.2) = 2,9
⇒ M = Ba