Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi x, y tương ứng là số mol Mg và MgO: 24x + 40y = 8,8.
x + y = nMgCl2 = 28,5/95 = 0,3
Giải hệ thu được: x = 0,2; y = 0,1.
a) %Mg = 24.0,2/8,8 = 54,54%; %MgO = 100 - 54,54 = 45,46%
b) nHCl = 2(x+y) = 0,6 mol; mdd =36,5.0,6.100/14,6 = 150 gam.
c) mdd sau p.ư = 8,8 + 150 - mH2 = 158,8 - 2.0,2 = 158,4 gam.
%MgCl2 = 28,5/158,4 = 17,99%

%O = 100% - 68,852% - 4,918% = 26,23%
Gọi công thức của A là C x H y O z
Ta có:
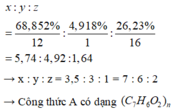
Mặt khác ta có M x < 200 → 122n < 200
→ n = 1
→ X có công thức phân tử là C 7 H 6 O 2 , A có khả năng tham gia phản ứng tráng bạc và phản ứng được với NaOH
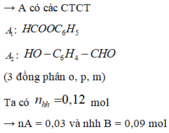
A 1 phản ứng với KOH cho 2 muối HCOOK: 0,03 mol và C 6 H 5 OK : 0,03mol
B phản ứng với KOH cho muối KO - C 6 H 4 - CHO : 0,09 mol
→ m muối = 20,85 gam
Đáp án D

Đáp án D
![]()
![]()
Ta thấy ![]() dư , Fe và Al hết. Chất rắn còn lại là Cu.
dư , Fe và Al hết. Chất rắn còn lại là Cu.
Gọi ![]()
![]()
Quá trình cho – nhận e:
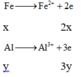
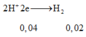
Theo bảo toàn e ta có: 2x + 3y = 0,04 (2)
Từ (1) và (2)
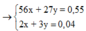
![]()
=> trong cốc sau phản ứng với H 2 S O 4 có :
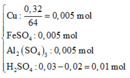
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()

![]() phản ứng vừa đủ.
phản ứng vừa đủ.
![]()
![]() lit
lit
Trong dung dịch sau phản ứng gồm: ![]()
m
m
u
ố
i
= ![]()
= 0,87 + 0,03.96 + 0,005.23 = 3,865 g



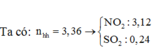

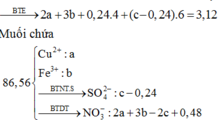




Ta có nFeO = \(\dfrac{7,2}{72}\) = 0,1 ( mol )
nH2SO4 = \(\dfrac{100\times20\%}{98}\) = 0,2 ( mol )
FeO + H2SO4 \(\rightarrow\) FeSO4 + H2O
0,1.......0,2
=> Lập tỉ số \(\dfrac{0,1}{1}:\dfrac{0,2}{1}\) = 0,1 < 0,2
=> Sau phản ứng FeO hết , H2SO4 dư
=> mH2SO4 tham gia phản ứng = 0,1 . 98 = 9,8 ( gam )
=> mFeSO4 = 152 . 0,1 = 15,2 ( gam )
Mdung dịch = Mtham gia
= 100 + 7,2 = 107,2 ( gam )
=> C%FeSO4 = \(\dfrac{15,2}{107,2}\) . 100 \(\approx\) 14,18%