Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nkhí = 4,48 : 22,4 = 0,2 (mol);
nAl2O3 = 15,3 : 102 = 0,15 (mol)
Có thể xảy ra:
Catot:
Cu2+ + 2e → Cu (1)
2H2O + 2e → 2OH- + H2↑ (2)
Anốt
Cl- → Cl2 +2e (3)
2H2O → 4H+ + O2 +4e (4)
Vì Al2O3 có thể bị hòa tan bởi OH- hoặc H+ nên có thể xảy ra 2 trường hợp sau:
TH1: Bên anot nước bị điện phân trước, không có (2) xảy ra.
Al2O3 + 6H+ → 2Al3+ + 3H2O
0,15→ 0,9 (mol)
=> nO2 = 1/4nH+ = 0,225 (mol) > 0,2 mol khí => loại
TH2: Bên catot nước bị điện phân trước, không có (4)
=> nCl2 = nkhí = 0,2 (mol) => ne trao đổi = 2nCl2 = 0,4 (mol)
Al2O3 + 2OH- → 2AlO2- + 2H2O
0,15→ 0,3 (mol)
=> nCu2+ = (0,4 – 0,3)/ 2 = 0,05 (mol)
=> m = mCuSO4 + mKCl = 0,05. 160 + 0,4. 74,5 = 37,8 (g)
Đáp án A

Đáp án A
nkhí = 4,48 : 22,4 = 0,2 (mol); nAl2O3 = 15,3 : 102 = 0,15 (mol)
Có thể xảy ra:
Catot: Anốt
Cu2+ + 2e → Cu (1) Cl- → Cl2 + 2e (3)
2H2O + 2e → 2OH- + H2↑ (2) 2H2O → 4H+ + O2 + 4e (4)
Vì Al2O3 có thể bị hòa tan bởi OH- hoặc H+ nên có thể xảy ra 2 trường hợp sau:
TH1: Bên anot nước bị điện phân trước, không có (2) xảy ra.
Al2O3 + 6H+ → 2Al3+ + 3H2O
0,15→ 0,9 (mol)
=> nO2 = 1/4nH+ = 0,225 (mol) > 0,2 mol khí => loại
TH2: Bên catot nước bị điện phân trước, không có (4)
=> nCl2 = nkhí = 0,2 (mol) => ne trao đổi = 2nCl2 = 0,4 (mol)
Al2O3 + 2OH- → 2AlO2- + 2H2O
0,15→ 0,3 (mol)
=> nCu2+ = (0,4 – 0,3)/ 2 = 0,05 (mol)
=> m = mCuSO4 + mKCl = 0,05. 160 + 0,4. 74,5 = 37,8 (g)

Chọn C.
Dung dịch Y chứa H+ với n H + = 2 n H 2 = 0 , 12 mol ⇒ H + ban đầu: 0 , 12 + 2 n H 2 ⇒ n O 2 = 0 , 03 + 0 , 5 n H 2
Khối lượng dung dịch giảm:
m Cu + m khí = 300 - 283 , 32 = 16 , 68 ⇒ 64 n Cu + 71 n Cl 2 + 18 n H 2 = 15 , 72 (1)
→ BT : e 2 n Cu = 0 , 12 + 2 n Cl 2 (2) và
160 n Cu + 117 n Cl 2 = 31 , 76 (3)
Từ (1), (2), (3) suy ra:
n Cu = 0 , 14 mol ; n Cl 2 = 0 , 08 mol ; n H 2 = 0 , 06 mol ⇒ n O 2 = 0 , 06 mol
Vậy V = 3,136 lít.

Đáp án B
Ta có: ![]()
Điện phân X đến khi dung dịch giảm 24,88 gam thì dừng. Dung dịch thu được 2 chất tan. Cho Mg vào Y thấy thành Mg giảm 3,36 gam chứng tỏ có H+.
Do vậy hai chất tan trong Y là H2SO4 và Na2SO4
![]()
Cu2+ bị điện phân hết và có sinh ra 0,28 mol H+
=> 
Dung dịch bị giảm do Cu2+, Cl- và H2O bị điện phân.
![]()
![]()
Giải được: x=0,01.
Vậy ở anot thu được 0,1 mol Cl2 và 0,075 mol O2.
![]()

Giải thích: Đáp án C
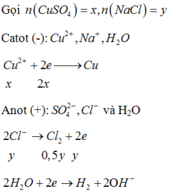
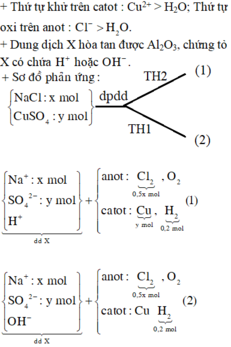
Do dung dịch X là phenol phâtlein hóa hồng nên dung dịch X có MT bazơ nên dung dịch sau phản ứng hòa tan Al2O3 là OH-; (H2O đã điện phân bên catot, còn anot chưa đp H2O)
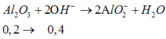
Suy ra n(Cl2) = n (khí anot) = 0,4=0,5y; vậy y=0,8
Bảo toàn e có n(e trao đổi) = 2x+0,4=y=0,8, nên x=0,2
Vậy m = 160.0,2 + 58,5.0,8 = 78,8
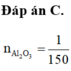
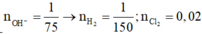

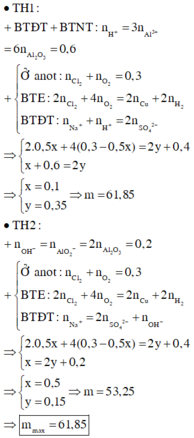

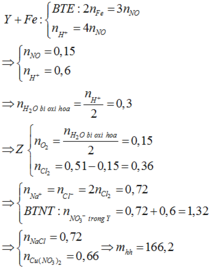
Đáp án B
nNaCl = 1mol
Do đó sau khi NaCl bị điện phân hết thì tiếp tục có sự điện phân nước:
Khi đó khí thoát ra ở anot gồm có Cl2 và O2