Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

Em tham khảo nhé !
Đặt nAl = a và nFe = b
—> 27a + 56b = 3,28 (1)
nHCl = 0,5 và nNaOH = 0,65
—> nNaCl = 0,5
TH1: Nếu kết tủa vẫn còn Al(OH)3 —> nNaAlO2 = 0,65 – 0,5 = 0,15
Kết tủa gồm Fe(OH)2 (b) và Al(OH)3 (a – 0,15)
Nung ngoài không khí —> Al2O3 (a – 0,15)/2 và Fe2O3 (b/2)
m rắn = 102(a – 0,15)/2 + 160b/2 = 1,6 (2)
(1)(2) —> Vô nghiệm, loại
TH2: Kết tủa chỉ có Fe(OH)2 (b mol)
—> m rắn = 160b/2 = 1,6 (3)
(1)(3) —> a = 0,08 và b = 0,02
—> %Al = 65,85% và %Fe = 34,15%

Pư: Mg+2HCl -> MgCl2 +H2
MgO+2HCl-> MgCl2 +H2O
MgCl2+2NaOH-> Mg(OH)2↓+2NaCl
Mg(OH)2-> MgO+H2O
nMgO=14/40=0.35 mol
-> nMg(OH)2=nMgCl2=nMgO=0.35 mol
-> nMgO=nMg=nMgCl2=0.35 mol
gọi x,y lần lượt là số mol của Mg,MgO
->mhh=24x+40y=2 (1)
nMgCl2=x+y=0.35 (2)
giải hệ (1)(2) có x=0.103125
y=0.246875
- khối lượng của bạn nhập sai vì klg hỗn hợp quá nhỏ

Bài giải:
2Fe + 6H2SO4 -> Fe2(SO4)3 + 3SO2 + 6H2O
2Al + 6H2SO4 -> Al2(SO4)3 + 3SO2 + 6H2O
Cu + 2H2SO4 -> CuSO4 + SO2 + 2H2O
(chú ý là H2SO4 đặc, nóng sẽ khử kim loại tạo muối sunfat kim loại có hóa trị cao nhất)
Lượng 3 muối sunfat = 45,1.2 = 90,2 gam và số mol SO2 = 0,7 mol
Fe2(SO4)3 + 6NaOH -> 2Fe(OH)3 + 3Na2SO4
Al2(SO4)3 + 6NaOH -> 2Al(OH)3 + 3Na2SO4
CuSO4 + 2NaOH -> Cu(OH)2 + Na2SO4
Al(OH)3 + NaOH -> NaAlO2 + H2O
Kết tủa lọc được chỉ còn Fe(OH)3 và Cu(OH)2
2Fe(OH)3 -> Fe2O3 + 3H2O
Cu(OH)2 -> CuO + H2O
12.2 = 24 (gam) là tổng lượng 2 oxit Fe2O3 + CuO
Gọi x, y, z lần lượt là số mol của Fe, Al, Cu
Ta có hệ 3 phương trình:
1,5x + 1,5y + z = 0,7
200x + 171y + 160z = 90,2
80x + 80z = 24
Giải hệ cho x = 0,2 ; y = 0,2 ; z = 0,1
Suy ra khối lượng mỗi kim loại trong hỗn hợp ban đầu: mFe = 11,2 g ; mAl = 5,4 g ; mCu = 6,4 g
\\ok//
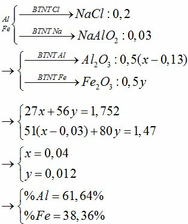
Gọi số mol của Al là : x
số mol của Fe là : y
Ta có : 1500ml = 1,5l
nH2SO4 = 1,5.2 = 3 (mol)
mKOH = 800.43,75% = 350 (g)
nKOH = \(\frac{350}{56}=6,25\) (mol)
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
x -> 2x /mol
Fe + H2SO4 -> FeSO4 + H2
y -> y /mol
-> X gồm Al2(SO4)3 , FeSO4 và H2SO4 dư (có thể có)
Al2(SO4)3 + 6KOH -> 3K2SO4 + 2Al(OH)3
2x -> x /mol
FeSO4 + 2KOH -> K2SO4 + Fe(OH)2
y -> y /mol
H2SO4 + 2KOH -> K2SO4 + 2H2O
Bảo toàn SO4 : nH2SO4 = nK2SO4 = 3 (mol)
Theo pt ta thấy : nKOH = 2 . nK2SO4 = 3.2 = 6 (mol)
Ta có : nKOH đã p/ứ < nKOH tham gia p/ứ (6 < 6,25)
-> KOH còn dư
nKOH dư = 6,25 - 6 = 0,25 (mol)
Khi đó sẽ xảy ra thêm 1 phản ứng
KOH + Al(OH)3 -> KAlO2 + 2H2O
0,25 -> 0,25 /mol
nAl(OH)3 = x - 0,25 (mol)
Sau các phản ứng thì kết tủa gồm Al(OH)3 x-0,25 mol và Fe(OH)2 y mol
4Fe(OH)2 + O2 -> 2Fe2O3 + 4H2O
y -> y/2 /mol
2Al(OH)3 -> Al2O3 + 3H2O
x - 0,25 -> \(\frac{x-0,25}{2}\) /mol
Ta có hệ phương trình : \(\left\{{}\begin{matrix}\frac{160y}{2}+\frac{102\left(x-0,25\right)}{2}=40\\56y+27x=36,1\end{matrix}\right.\)
Giải hệ ta có : x = 0,095 ; y = 0,599
mAl = 0,095.27 =2,565 (g)
mFe = 36,1 - 2,565 = 33,535