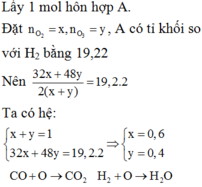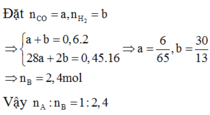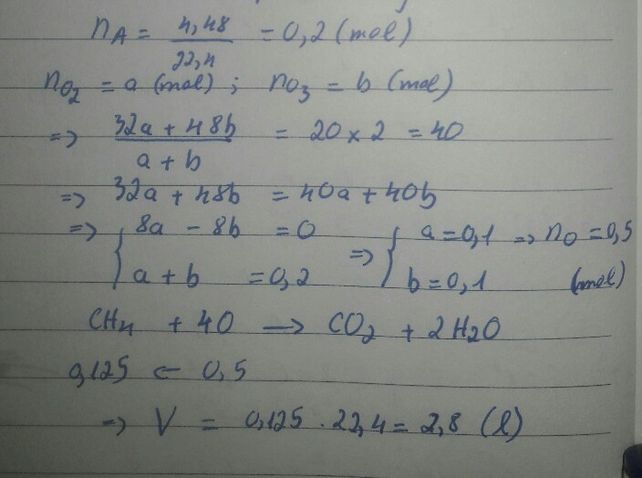Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH của các phản ứng :
2CO + O 2 → 2C O 2 (1)
3CO + O 3 → 3C O 2 (2)
Trong 1 mol hỗn hợp khí A có 0,6 mol O 3 và 0,4 mol O 2
Theo (1): 0,6 mol O 2 đốt cháy được 1,2 mol CO.
Theo (2) : 0,4 mol O 3 đốt cháy được 1,2 mol CO.
Kết luận : 1 mol hỗn hợp khí A đốt cháy được 2,4 mol khí CO.

Gọi a,b lần lượt là số mol của O2 và O3
=> \(\dfrac{32a+48b}{a+b}=22.2=44\)
\(\Leftrightarrow32a+48b=44a+44b\)
\(\Leftrightarrow12a=4b\)
=> b=3a
=> %VO2 = \(\dfrac{a}{a+3a}.100\%=25\%\), %VO3 = 75%
b) Thể tích O2 trong 2,24 lít khí là: 25%.2,24 = 0,56 lít
thể tích O3 = 1,68 lít
=> nO2 = \(\dfrac{0,56}{22,4}=0,025mol\Rightarrow mO_2=0,8g\)
\(nO_3=\dfrac{1,68}{22,4}=0,075mol\Rightarrow mO_3=0,075.48=3,6g\)

Đặt a,b lần lượt là số mol của O2, O3 trong hh
\(M_{hh}=20.2=40\left(\dfrac{g}{mol}\right)\\ M_{hh}=\dfrac{32a+48b}{a+b}=40\\ \Leftrightarrow40a+40b=32a+48b\\ \Leftrightarrow8a=8b\\ \Leftrightarrow\dfrac{a}{b}=\dfrac{1}{1}\)
=> tỉ lệ số mol trong hh trên giữa O2 và O3 là 1:1
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ C_2H_4O_2+2O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\\ n_{O_2}=2.\left(n_{CH_4}+n_{C_2H_4O_2}\right)=2.\left(1+1\right)=4\left(mol\right)\\ \Rightarrow n_X=n_{O_2}.2=4.2=8\left(mol\right)\)
Em nghĩ chưa đúng đâu chị, tại căn bản là hỗn hợp khí có 2 khí oxi và ozon thì mình không nên giả sử ạ!

Gọi \(\left\{{}\begin{matrix}n_{O2}:a\left(mol\right)\\n_{O3}:b\left(mol\right)\end{matrix}\right.\)
\(\Leftrightarrow\frac{32a+48b}{a+b}=17,62\)
\(\Leftrightarrow12,8b=3,2a\Leftrightarrow a=4b\)
Vì thể tích tỉ lệ với số mol
\(\%V_{O2}=\frac{a}{a+b}.100\%=\frac{4b}{4b+b}.100\%=80\%\)
\(\Rightarrow\%V_{O3}=100\%-80\%=20\%\)
5,04 l khí A chứa:
\(\left\{{}\begin{matrix}n_{O2}=\frac{5,04.80\%}{22,4}=0,18\left(mol\right)\\n_{O3}=\frac{5,04.20\%}{22,4}=0,045\left(mol\right)\end{matrix}\right.\)
\(2O_3\underrightarrow{^{t^o}}3O_2\)
0,045_0,0675_
\(\Rightarrow\Sigma n_{O2}=0,18+0,0675=0,2475\left(mol\right)\)
\(CH_4+2O_2\rightarrow CO_2+H_2O\)
0,12375__0,2475 ______
\(\Rightarrow V_{CH4}=0,12375.22,4=2,772\left(l\right)\)

Đáp án A.
Coi số mol hỗn hợp X = 1 mol
n O 2 = X , n O 3 = Y ( m o l )
→ x + y = 1 32 x + 48 y = 1 . 19 , 2 . 2
→ x = 0,6 , y = 0,4 (mol)
→ % V O 2 = 60 % , % V O 3 = 40 %

Đặt x và y là số mol O 3 và O 2 có trong 1 mol hỗn hợp khí
Hỗn hợp khí A : (48x + 32y)/(x+y) = 19,2 x 2 = 38,4
→ 3x = 2y → 40% O 3 và 60% O 2
Đặt x và y là số mol H 2 và CO có trong 1 mol hỗn hợp khí
Hỗn hợp khí B : (2x + 28y)/(x+y) = 3,6 x 2 = 7,2
→ x = 4y → 80% H 2 và 20% CO