Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

A với c: S có cả tính khử và tính oxi hóa
B với d: SO2 là chất khí có tính oxi hóa và tính khử
C với b: H2S chỉ có tính khử
D với a: H2SO4 chỉ có tính oxi hóa

Đáp án D
S là đơn chất vừa có tính khử vừa có tính oxi hoá => (1) – (c)
SO2 là hợp chất vừa có tính oxi hoá vừa có tính khử => (2) – (d)
H2S là hợp chất chỉ có tính khử => (3) – (b)
H2SO4 là hợp chất có tính axit và tính oxi hoá mạnh => (40) – (a)

Số mol hỗn hợp khí X:
n(X) = n(Cl2) + n(O2) = 11,2/22,4 = 0,5mol [1]
Theo ĐL bảo toàn khối lượng:
m(X) + m(Y) = m(Z) ⇒ m(X) = m(Cl2) + m(O2) = m(Z) - m(Y) = 42,34 - 16,98
⇒ 71.n(Cl2) + 32.n(O2) = 25,36 [2]
Từ [1], [2] ⇒ n(Cl2) = 0,24mol và n(O2) = 0,26mol
Phần trăm thể tích của oxi trong X:
%O2 = V(O2)/V(X) .100% = 0,26.22,4/11,2 .100% = 52%

Chúng ta sẽ sử dụng axit ví dụ như HCl cho tác dụng với kẽm để thu được vàng tinh khiết

Đối với các nguyên tố thuộc các nhóm A thì những electron ở lớp ngoài cùng quyết định tính chất hoá học của nguyên tố tương ứng.
Các electron ở lớp ngoài cùng có khả năng, tham gia hình thành liên kết hoá học được gọi là các electron hoá trị.
Thí dụ, cacbon có cấu hình electron : 1 s 2 2 s 2 2 p 2 , các electron 2 s 2 2 p 2 là những electron lớp ngoài cùng và là những electron hoá trị.

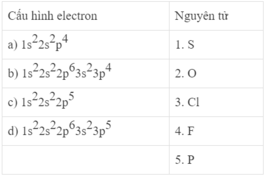

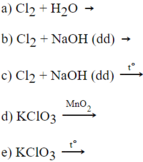
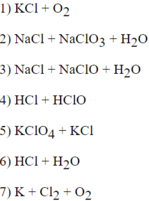
1-c; 2-e; 3-b; 4-a