Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(m_S=m_B-m_{hh\left(bđ\right)}=29,55-15,15=14,4\left(g\right)\)
b) \(n_S=\dfrac{14,4}{32}=0,45\left(mol\right)\)
Kết tủa thu được là Ag2S
Bảo toàn S: \(n_{Ag_2S}=0,45\left(mol\right)\)
=> \(m_{Ag_2S}=0,45.248=111,6\left(g\right)\)

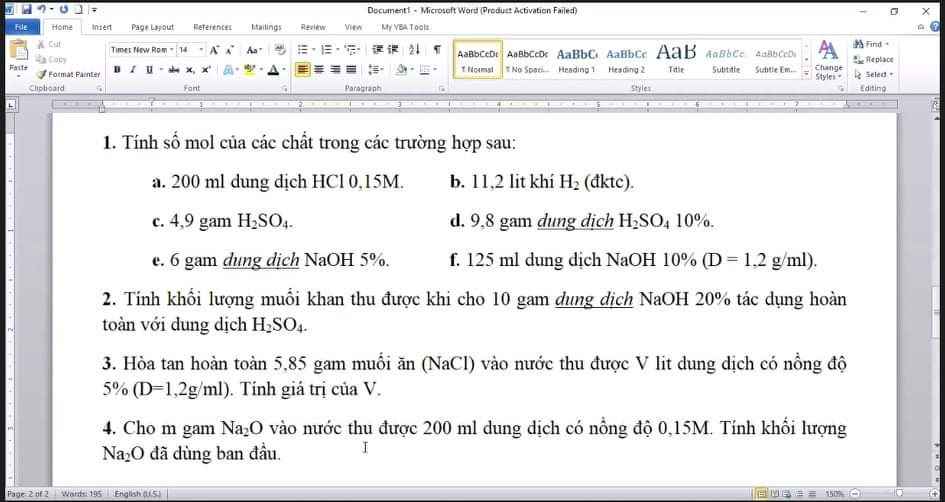
1.
a.\(n_{HCl}=0,2.0,15=0,03\left(mol\right)\)
b.\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
c.\(n_{H_2SO_4}=\dfrac{4,9}{98}=0,05\left(mol\right)\)
d.\(m_{H_2SO_4}=10\%.9,8=0,98\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{0,98}{98}=0,01\left(mol\right)\)
e.\(m_{NaOH}=6.5\%=0,3\left(g\right)\Rightarrow n_{NaOH}=\dfrac{0,3}{40}=0,0075\left(mol\right)\)
f.\(m_{ddNaOH}=125.1,2=150\left(g\right)\Rightarrow m_{NaOH}=150.20\%=30\left(g\right)\)
\(\Rightarrow n_{NaOH}=\dfrac{30}{40}=0,75\left(mol\right)\)
2.
\(m_{NaOH}=10.20\%=2\left(g\right)\Rightarrow n_{NaOH}=\dfrac{2}{40}=0,05\left(mol\right)\)
PTHH: 2NaOH + H2SO4 → Na2SO4 + H2O
Mol: 0,05 0,025
\(\Rightarrow m_{Na_2SO_4}=0,025.142=3,55\left(g\right)\)
3.
\(n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\)
PTHH: 2NaCl + 2H2O → 2NaOH + Cl2 + H2
Mol: 0,1 0,1
\(m_{NaOH}=0,1.40=4\left(g\right)\Rightarrow m_{ddNaOH}=\dfrac{4.100\%}{5\%}=80\left(g\right)\)
\(\Rightarrow V_{ddNaOH}=\dfrac{80}{1,2}=66,7\left(ml\right)\)

a) Gọi số mol Zn, Al là a, b (mol)
=> 65a + 27b = 1,84 (1)
PTHH: Zn + 2HCl --> ZnCl2 + H2
a--------------->a----->a
2Al + 6HCl --> 2AlCl3 + 3H2
b-------------->b----->1,5b
=> 136a + 133,5b = 5,39 (2)
(1)(2) => a = 0,02 (mol); b = 0,02 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,02.65}{1,84}.100\%=70,65\%\\\%m_{Al}=\dfrac{0,02.27}{1,84}.100\%=29,35\%\end{matrix}\right.\)
b) nH2 = a + 1,5b = 0,05 (mol)
=> VH2 = 0,05.22,4 = 1,12 (l)

nKMnO4 = 14,2/158 ≃ 0,0899 mol
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,0899 \(\dfrac{0,0899\times5}{2}\)
→ nCl2 = 0,22475 mol → VCl2 = 22,4.nCl2 = 5,0344 lít

Ta có: \(\left\{{}\begin{matrix}p+e+n=52\\p=e\\n-p=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=17\\n=18\end{matrix}\right.\)

\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_S=\dfrac{0,8}{32}=0,025\left(mol\right)\)
PTHH: Fe + S --to--> FeS
LTL: \(0,1>0,025\rightarrow\) Fe dư
Theo pthh: \(n_{Fe\left(pu\right)}=n_{FeS}=n_S=0,025\left(mol\right)\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe\left(du\right)}=\left(0,1-0,025\right).56=4,2\left(g\right)\\m_{FeS}=0,025.88=2,2\left(g\right)\end{matrix}\right.\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
0,075 0,075
FeS + 2HCl ---> FeCl2 + H2S
0,025 0,025
\(\rightarrow\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,075}{0,075+0,025}=75\%\\\%V_{H_2S}=100\%-75\%=25\%\end{matrix}\right.\)

- Trích một ít các dd làm mẫu thử, đánh số thứ tự lần lượt
- Cho các dd tác dụng với giấy quỳ tím:
+ QT chuyển đỏ: AgNO3
+ QT chuyển xanh: Na2S, Na2CO3 (1)
+ QT không chuyển màu: K2SO4, KCl (2)
- Cho các dd ở (1) tác dụng với dd HCl dư
+ Có khí mùi trứng thối thoát ra: Na2S
Na2S + 2HCl --> 2NaCl + H2S
+ Có khí không mùi thoát ra: Na2CO3
Na2CO3 + 2HCl --> 2NaCl + CO2 + H2O
- Cho các dd ở (2) tác dụng với dd BaCl2
+ Không hiện tượng: KCl
+ Kết tủa trắng: K2SO4
\(K_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2KCl\)