
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


d) Gọi x,y lần lượt là số mol Al, Fe
\(\left\{{}\begin{matrix}27x+56y=8,3\\1,5x+y=0,25\end{matrix}\right.\)
=> x=0,1 ; y=0,1
Kết tủa : Al(OH)3, Fe(OH)2
Bảo toàn nguyên tố Al: \(n_{Al\left(OH\right)_3}=n_{Al}=0,1\left(mol\right)\)
Bảo toàn nguyên tố Fe: \(n_{Fe\left(OH\right)_2}=n_{Fe}=0,1\left(mol\right)\)
=> \(m=0,1.78+0,1.90=16,8\left(g\right)\)
Nung kết tủa thu được chất rắn : Al2O3 và FeO
Bảo toàn nguyên tố Al: \(n_{Al_2O_3}.2=n_{Al}\Rightarrow n_{Al_2O_3}=0,05\left(mol\right)\)
Bảo toàn nguyên tố Fe: \(n_{FeO}=n_{Fe}=0,1\left(mol\right)\)
=> \(a=0,05.102+0,1.72=12,3\left(g\right)\)

PTHH: Al2O3+6HCl➝2AlCl3+3H2O(1)
a)nAl2O3=\(\dfrac{10,2}{102}\)=0,1(mol)
mHCl=\(\dfrac{5\%.219}{100\%}\)=10,95(g)
⇒nHCl=\(\dfrac{10,95}{36,5}\)=0,3(mol)
Xét tỉ lệ Al2O3:\(\dfrac{0,1}{1}\)=0,1
Xét tỉ lệ HCl:\(\dfrac{0,3}{6}\)=0,05
⇒HCl pứng hết,Al2O3 còn dư
Theo PTHH(1) ta có nAl2O3 pứng=\(\dfrac{nHCl}{6}\)=\(\dfrac{0,3}{6}\)=0,05(mol)
⇒nAl2O3 dư=nAl2O3ban đầu-nAl2O3 pứng=0,1-0,05=0,05(mol)
⇒mAl2O3 dư=0,05.102=5,1(g)
b) C%HCl=\(\dfrac{0,3.36,5}{219+10,2}\).100%=4,8%
nAlCl3=0,1(mol)
⇒C%AlCl3=\(\dfrac{0,1.136,5}{10,2+219}\).100%=6%


1.
\(n_{KNO_3}=0.15\cdot0.1=0.015\left(mol\right)\)
\(m_{KNO_3}=0.015\cdot101=1.515\left(g\right)\)
2.
\(m_{KOH}=200\cdot20\%=40\left(g\right)\)
Sau khi pha :
\(m_{dd_{KOH}}=\dfrac{40}{16\%}=250\left(g\right)\)
\(m_{H_2O\left(tv\right)}=250-200=50\left(g\right)\)
3.
\(n_{NaOH}=2\cdot1=2\left(mol\right)\)
Sau khi pha :
\(V_{dd_{NaOH}}=\dfrac{2}{0.1}=20\left(l\right)\)
\(V_{H_2o\left(tv\right)}=20-2=18\left(l\right)\)
3)
$n_{KNO_3} = 0,15.0,1 = 0,015(mol)$
$m_{KNO_3} = 0,015.101 = 1,515(gam)$
4)
$m_{KOH} = 200.20\% = 40(gam)$
$m_{dd\ KOH\ 16\%} = \dfrac{40}{16\%} = 250(gam)$
$\Rightarrow m_{H_2O} = 250 -200= 50(gam)$
5)
$n_{NaOH} = 2.1 = 2(mol)$
$V_{dd\ NaOH} = \dfrac{2}{0,1} = 20(lít)$
$\Rightarrow V_{H_2O} = 20 - 2 = 18(lít)$
4)



Bài 4:
a)
- Hòa tan 3 chất rắn vào dd NaOH
+ Chất rắn tan, sủi bọt khí: Al
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
+ Chất rắn không tan: Fe, Cu
- Hòa tan 2 chất rắn còn lại vào dd HCl
+ Chất rắn tan, sủi bọt khí: Fe
Fe+ 2HCl --> FeCl2 + H2
+ Chất rắn không tan: Cu
b)
- Hòa tan 4 chất rắn vào nước:
+ Chất rắn tan: CaO
CaO + H2O --> Ca(OH)2
+ Chất rắn không tan: CuO, MgO, Al2O3
- Hòa tan 3 chất rắn còn lại vào dd NaOH
+ Chất rắn tan: Al2O3
Al2O3 + 2NaOH --> 2NaAlO2 + H2O
+ Chất rắn không tan: CuO, MgO
- Hòa tan 2 chất rắn còn lại vào dd HCl:
+ Chất rắn tan, tạo dd màu xanh: CuO
CuO + 2HCl --> CuCl2 + H2O
+ Chất rắn tan, tạo dd trong suốt: MgO
MgO + 2HCl --> MgCl2 + H2O
c)
- Cho 3 dd tác dụng với dd NaOH dư
+ Xuất hiện kết tủa trắng, sau đó tan: AlCl3
AlCl3 + 3NaOH --> Al(OH)3 + 3NaCl
NaOH + Al(OH)3 --> NaAlO2 + 2H2O
+ Xuất hiện kết tủa trắng, không tan: MgCl2
MgCl2 + 2NaOH --> Mg(OH)2 + 2NaCl
+ Xuất hiện kết tủa nâu đỏ: FeCl3
d)
- Cho quỳ tím tác dụng với 4 dd
+ QT chuyển xanh: NaOH, Na2CO3 (1)
+ QT không chuyển màu: Na2SO4, NaNO3 (2)
- Cho dd BaCl2 tác dụng với 2 dd ở (1)
+ Kết tủa trắng: Na2CO3
Na2CO3 + BaCl2 --> BaCO3 + 2NaCl
+ Không hiện tượng: NaOH
- Cho dd BaCl2 tác dụng với 2 dd ở (2)
+ Kết tủa trắng: Na2SO4
Na2SO4 + BaCl2 --> BaSO4 + 2NaCl
+ Không hiện tượng: NaNO3
Bài 5
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
_____0,3<--------------------------0,3
=> mMg = 0,3.24 = 7,2 (g)
Gọi số mol Cu, Ag là a, b
=> 64a + 108b = 29,8-7,2 = 22,6(g)
PTHH: 2Mg + O2 --to--> 2MgO
_____0,3------------------>0,3
2Cu + O2 --to--> 2CuO
a------------------>a
=> 0,3.40 + 80a + 108b = 36,2
=> a = 0,1; b = 0,15
=> mCu = 0,1.64 = 6,4 (g)
=> mAg = 0,15.108 = 16,2 (g)

PTHH: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
Ta có: \(\left\{{}\begin{matrix}m_{H_2SO_4}=588\cdot5\%=29,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\\n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,3}{3}\) \(\Rightarrow\) Al2O3 còn dư
\(\Rightarrow n_{Al_2\left(SO_4\right)_3}=0,1\left(mol\right)=n_{Al_2O_3\left(dư\right)}\)
\(\Rightarrow C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,1\cdot342}{20,4+588-0,1\cdot102}\cdot100\%\approx5,72\%\)










 giúp mình với ạ , mình đang cần gấp ạ, các bạn làm theo cách kẻ bảng ra giúp mình được không ạ
giúp mình với ạ , mình đang cần gấp ạ, các bạn làm theo cách kẻ bảng ra giúp mình được không ạ
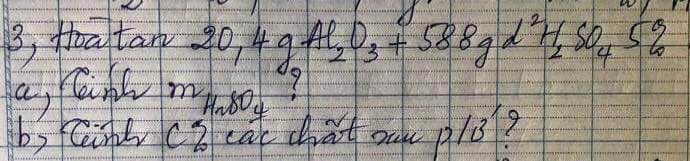
nNa2SO4= 9,94/142=0,07(mol);
mBa(OH)2= 20,52(g) -> nBa(OH)2=0,12(mol)
PTHH: Na2SO4 + Ba(OH)2 -> BaSO4 + 2 NaOH
Ta cps: 0,07/1 < 0,12/1
=> Ba(OH)2 dư, Na2SO4 hết, tính theo nNa2SO4.
-> nBaSO4=nNa2SO4= 0,07(mol)
=> m(kết tủa)=mBaSO4=0,07.233=16,31(g)
=>m=16,31(g)
b) Dung dịch A thu được bao gồm NaOH và Ba(OH)2 dư.
nNaOH=2.0,07=0,14(mol) => mNaOH= 0,14.40=5,6(g)
nBa(OH)2 (dư)=0,12-0,07=0,05(mol)
=> mBa(OH)2 (dư)= 0,05.171=8,55(g)
=> mddA=Na2SO4 + mddBa(OH)2 - mBaSO4 = 9,94+ 100 - 16,31= 93,63(g)
=> C%ddBa(OH)2 (dư)= (8,55/93,63).100=9,132%
C%ddNaOH= (5,6/93,63).100=5,981%
Cảm ơn ạ