
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a. Trọng lượng của vật là:
P=10.m= 10.15=150N
Trọng lực có phương thẳng đứng, chiều từ trên xuống dưới.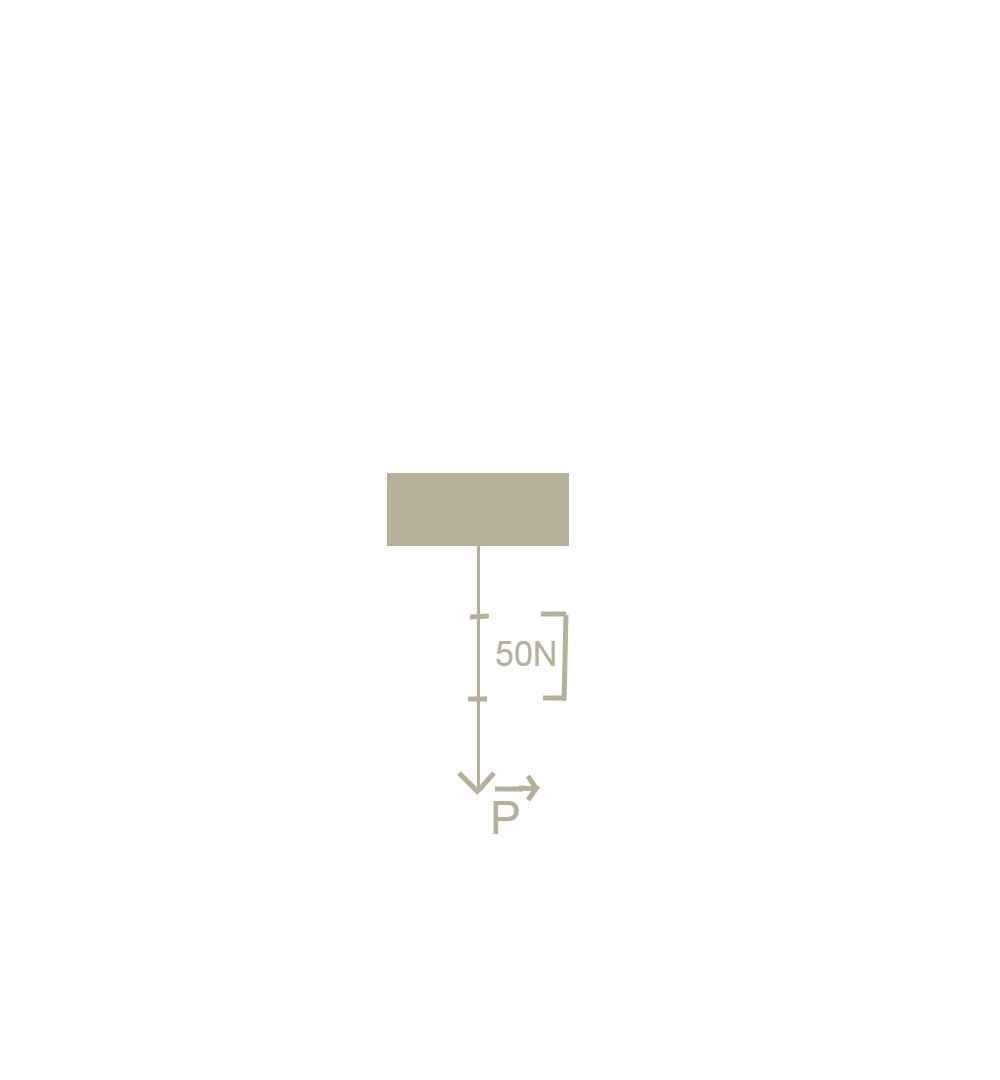 b.
b. 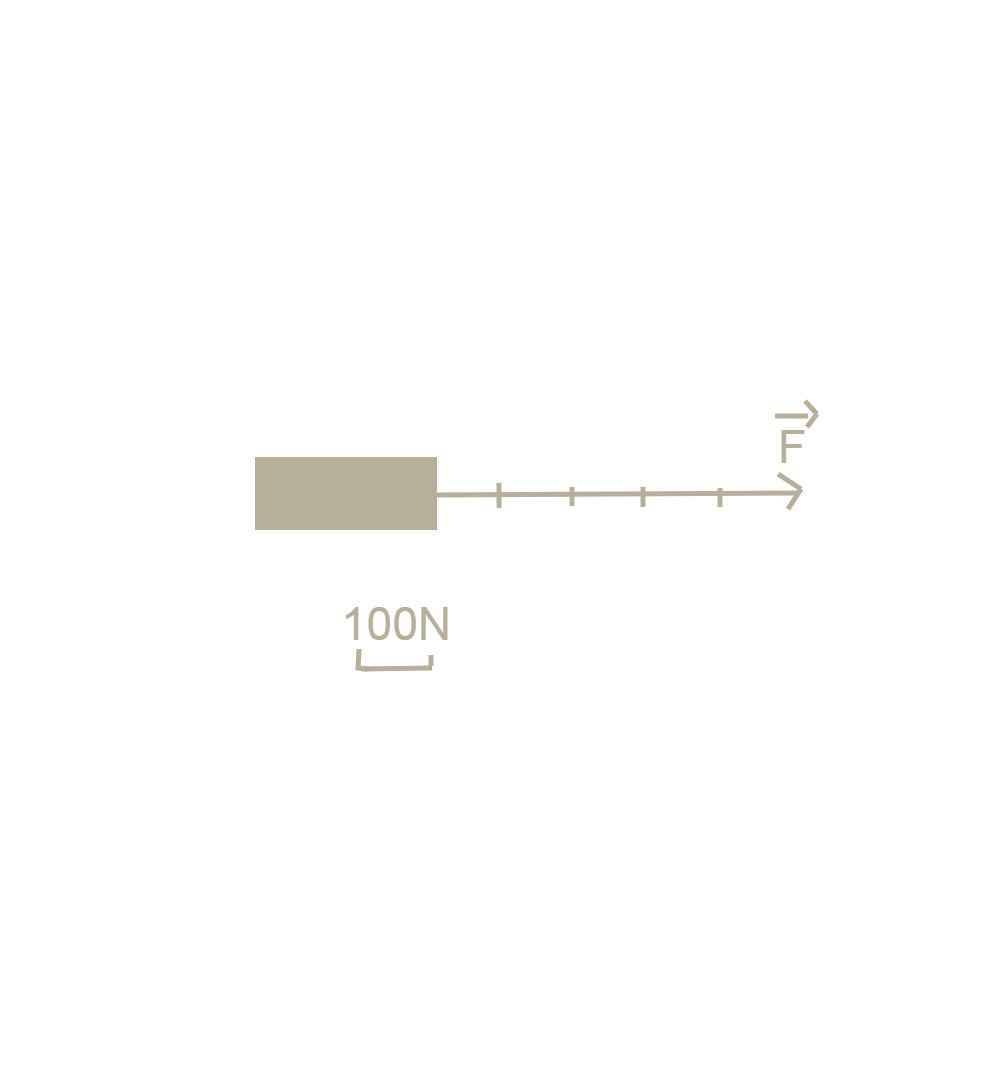 c.Trọng lượng của vật là:
c.Trọng lượng của vật là:
P= 10.m= 10.6=60N
Trọng lượng có phương thẳng, đứng chiều từ trên xuống dưới.
Vì vật đang đứng yên, nên chứng tỏ đã có 2 lực cân bằng tác dụng vào vật. Đó là trọng lực và lực nâng (P = Q)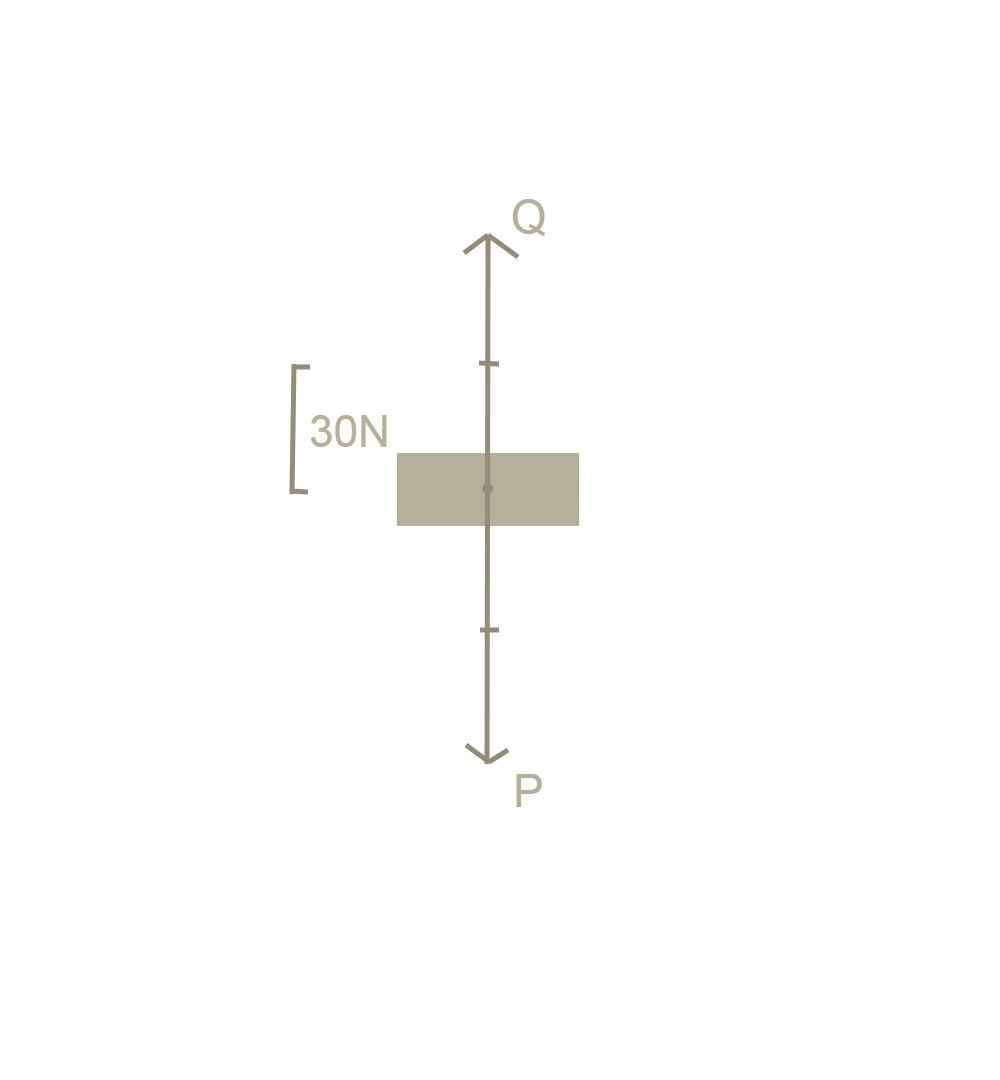

CTHH chung của hợp chất là \(Ba_x\left(PO_4\right)_y\left(x,y\in N\text{*}\right)\)
Theo QT hoá trị, ta có: \(x.II=y.III\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{2}\)
Mà \(x,y\in N\text{*}\)
\(\Rightarrow\left\{{}\begin{matrix}x=3\\y=2\end{matrix}\right.\)
Vậy CTHH của hợp chất là \(Ba_3\left(PO_4\right)_2\)
=> Chọn D

\(a.PTHH:Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(b.n_{Ba}=\dfrac{m}{M}=\dfrac{13,7}{137}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2O}=\dfrac{1}{2}.n_{Ba}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\\ \Rightarrow m_{H_2O}=n.M=0,9\left(g\right)\)
\(c.n_{Ba}=0,1\left(mol\right)\Rightarrow n_{H_2}=n_{Ba}=0,1\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=n.22,4=0,1.22,4=2,24\left(l\right)\)

Câu 3 :
Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Pt : Fe + H2SO4 → FeSO4 + H2\(|\)
1 1 1 1
0,1 0,1 0,1 0,1
a) Số mol của khí hidro
nH2 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,1 . 22,4
= 2,24 (l)
b) Số mol của muối sắt (II) sunfat
nFeSO4 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Khối lượng của muối sắt (II) sunfat
mFeSO4 = nFeSO4 . MFeSO4
= 0,1 . 152
= 15,2 (g)
c) Số mol của dung dịch axit sunfuric
nH2SO4 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
200ml = 0,2l
Nồng độ mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Chúc bạn học tốt
Câu 4 :
Số mol của photpho
nP = \(\dfrac{m_P}{M_P}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
Pt : 4P + 5O2 → (to) 2P2O5
4 5 2
0,2 0,25 0,1
a) Số mol của đi photpho pentaoxit
nP2O5 = \(\dfrac{0,2.2}{4}=0,1\left(mol\right)\)
Khối lượng của đi photpho pentaoxit
mP2O5 = nP2O5 . MP2O5
= 0,1 . 142
= 14,2 (g)
b) Số mol của khí oxi
nO2 = \(\dfrac{0,2.5}{4}=0,25\left(mol\right)\)
Thể tích của khí oxi ở dktc
VO2 = nO2 . 22,4
= 0,25 . 22,4
= 5,6 (l)
c) Pt : CH4 + 2O2 → CO2 + 2H2O\(|\)
1 2 1 2
0,25 0,125
Số mol của khí cacbonic
nCO2 = \(\dfrac{0,25.1}{2}=0,125\left(mol\right)\)
Thể tích của khí cacbonic ở dktc
VCO2 = nCO2 . 22,4
= 0,125 . 22,4
= 2,8 (l)
Chúc bạn học tốt

Bài 3 :
a) $Zn + 2HCl \to ZnCl_2 + H_2$
b) $n_{H_2} = n_{Zn} = \dfrac{6,5}{65} = 0,1(mol)$
$V_{H_2} = 0,1.22,4 = 2,24(lít)$
c) $n_{ZnCl_2} = n_{Zn} = 0,1(mol)$
$m_{ZnCl_2} = 136.0,1 = 13,6(gam)$
Bài 4 :
a) $2Zn + O_2 \xrightarrow{t^o} 2ZnO$
b)
$n_{Zn} = \dfrac{6,5}{65} = 0,1(mol)$
$n_{O_2} = \dfrac{1}{2}n_{Zn} = 0,05(mol)$
$V_{O_2} = 0,05.22,4 = 1,12(lít)$
c) $n_{ZnO} = n_{Zn} = 0,1(mol) \Rightarrow m_{ZnO} = 0,1.81 = 8,1(gam)$

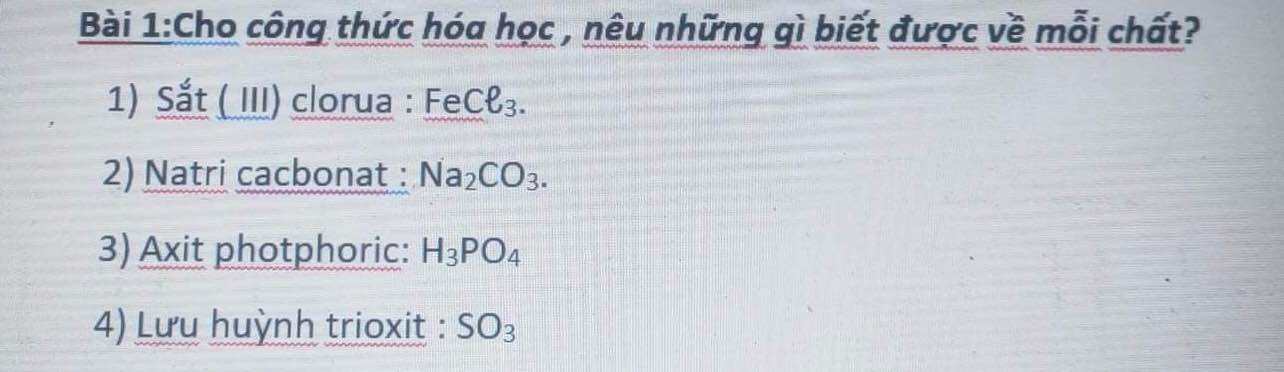
1.
- Hợp chất cấu tạo từ 2 nguyên tố: Fe và Cl
- Hợp chất có: 1 nguyên tố Fe và 3 nguyên tố Cl
- \(PTK=56+35,5\text{ x }3=162,5\left(đvC\right)\)
===========
2.
- Hợp chất cấu tạo từ 3 nguyên tố: Na, C và O
- Hợp chất có: 2 nguyên tố Na, 1 nguyên tố C và 3 nguyên tố O
- \(PTK=23\text{ x }2+12+16\text{ x }3=106\left(đvC\right)\)
==========
3.
- Hợp chất cấu tạo từ 3 nguyên tố: H, P và O
- Hợp chất có: 2 nguyên tố H, 1 nguyên tố P và 4 nguyên tố O
- \(PTK=1\text{ x }3+31+16\text{ x }4=98\left(đvC\right)\)
==========
4.
- Hợp chất cấu tạo từ 2 nguyên tố: S và O
- Hợp chất có: 1 nguyên tố S và 3 nguyên tố O
- \(PTK=32+16\text{ x }3=80\left(đvC\right)\)

Bài 1
CaCO3 \(\xrightarrow[]{t^o}\) CaO + CO2(1)
CO2 + 2NaOH \(\rightarrow\) Na2CO3 + H2O (2)
nCaCO3 = \(\dfrac{20}{100}=0,2mol\)
Theo pt (1) nCO2 = nCaCO3 = 0,2 mol
Theo pt (2) nNa2CO3 = nCO2 = 0,2mol
=> mNa2CO3 = 0,2.106 = 21,2g
Bài 1
CaCO3 CaO + CO2(1)
CO2 + 2NaOH Na2CO3 + H2O (2)
nCaCO3 =
Theo pt (1) nCO2 = nCaCO3 = 0,2 mol
nNaOH = 11,2 : 40 = 0,28 mol
Lập tỉ lệ : \(nCO_2:nNaOH=\dfrac{0,2}{1}:\dfrac{0,28}{2}=0,2:0,14\)
=> CO2 dư
nNa2CO3 = 1/2 n NaOH = 0,14mol
=> mNa2CO3 = 0,14.106 = 14,84g
Sửa lại xíu nha



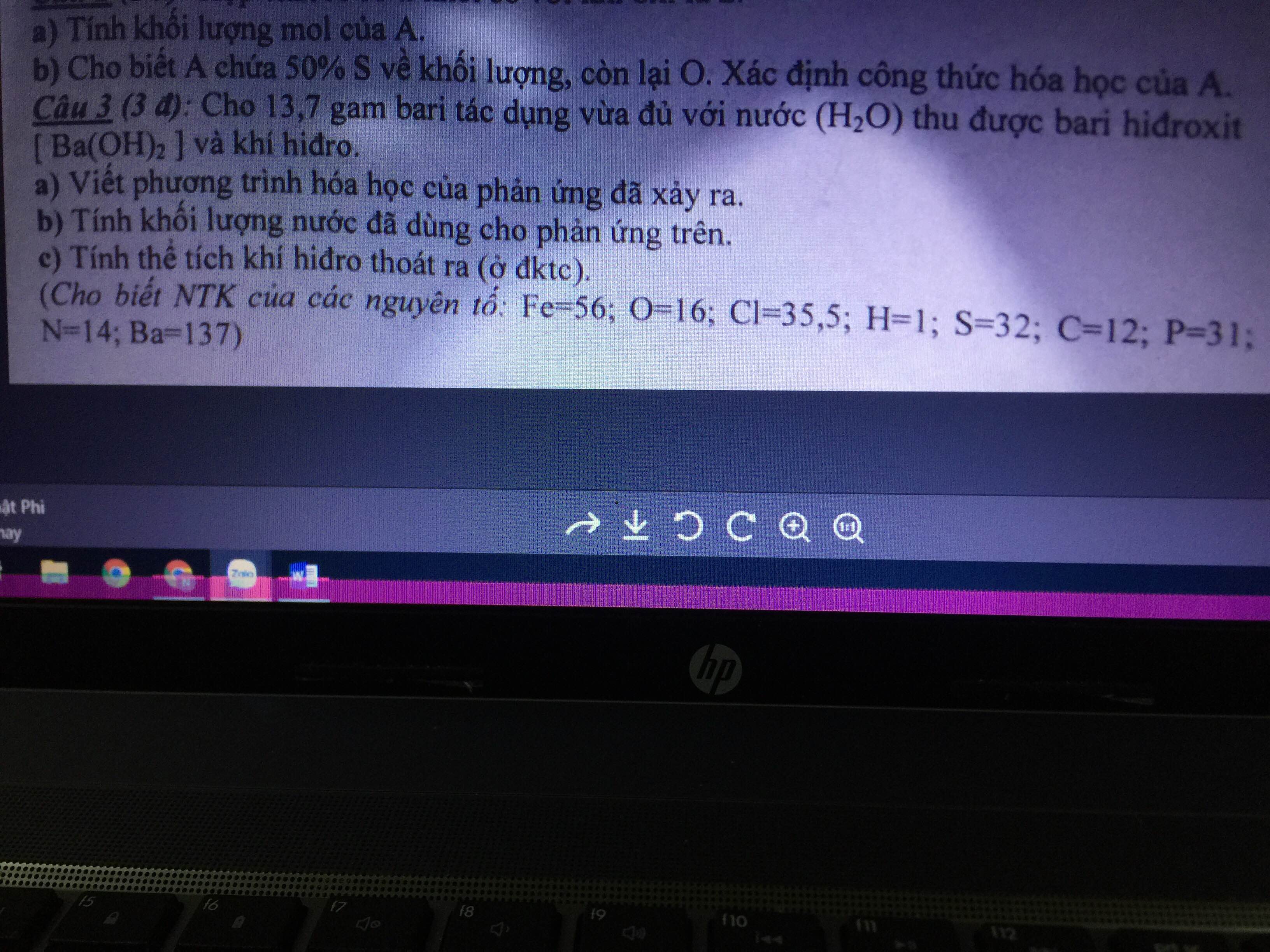


 Mn ơi, giải hộ mik câu này với! Tối nay mik phải nộp rồi ạ! Cảm ơn mn nhiều lắm!
Mn ơi, giải hộ mik câu này với! Tối nay mik phải nộp rồi ạ! Cảm ơn mn nhiều lắm!

