
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Bài 1.
a, PTPƯ: kẽm + axit clohidric → kẽm clorua + hidro
b, Theo ĐLBTKL ta có:
\(m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\)
c, Ta có: \(m_{HCl}=m_{ZnCl_2}+m_{H_2}-m_{Zn}=27,2+0,4-13=14,6\left(g\right)\)
Bài 2:
a, PTPƯ: metan + oxi → cacbon dioxit + hơi nước
b, Theo ĐLBTKL ta có:
\(m_{CH_4}+m_{O_2}=m_{CO_2}+m_{H_2O}\)
c, Ta có: \(m_{O_2}=m_{CO_2}+m_{H_2O}-m_{CH_4}=132+108-48=192\left(g\right)\)

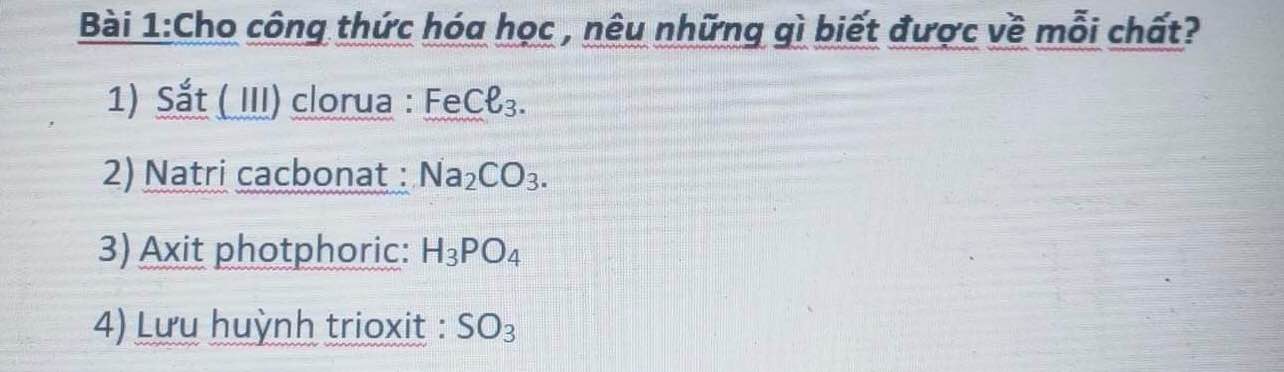
1.
- Hợp chất cấu tạo từ 2 nguyên tố: Fe và Cl
- Hợp chất có: 1 nguyên tố Fe và 3 nguyên tố Cl
- PTK=56+35,5 x 3=162,5(đvC)PTK=56+35,5 x 3=162,5(đvC)
===========
2.
- Hợp chất cấu tạo từ 3 nguyên tố: Na, C và O
- Hợp chất có: 2 nguyên tố Na, 1 nguyên tố C và 3 nguyên tố O
- PTK=23 x 2+12+16 x 3=106(đvC)PTK=23 x 2+12+16 x 3=106(đvC)
==========
3.
- Hợp chất cấu tạo từ 3 nguyên tố: H, P và O
- Hợp chất có: 2 nguyên tố H, 1 nguyên tố P và 4 nguyên tố O
- PTK=1 x 3+31+16 x 4=98(đvC)PTK=1 x 3+31+16 x 4=98(đvC)
==========
4.
- Hợp chất cấu tạo từ 2 nguyên tố: S và O
- Hợp chất có: 1 nguyên tố S và 3 nguyên tố O
- PTK=32+16 x 3=80(đvC)

Hi em, nhìn quả đề quen quá. Anh hỗ trợ rồi mà. Em có gì chưa hiểu bước nào thì hỏi lại nha em!

\(n_{Fe_2O_3}=\dfrac{24}{160}=0.15\left(mol\right)\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(0.15.........0.45............0.15\)
\(C_{M_{H_2SO_4}}=\dfrac{0.45}{0.2}=2.25\left(M\right)\)
\(m_{Fe_2\left(SO_4\right)_3}=0.15\cdot400=60\left(g\right)\)
\(C_{M_{Fe_2\left(SO_4\right)_3}}=\dfrac{0.15}{0.2}=0.75\left(M\right)\)

a)
\(n_{Fe_2O_3}=\dfrac{24}{160}=0,15\left(mol\right)\\ n_{H_2SO_4}=0,2.2,5=0,5\left(mol\right)\\ PTHH:Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O.\\ Vì:\dfrac{0,15}{1}< \dfrac{0,5}{3}\)
=> H2SO4 dư, Fe2O3 hết => Tính theo Fe2O3
Ta có:
\(n_{H_2SO_4\left(dư\right)}=0,5-\left(0,15.3\right)=0,05\left(mol\right)\\ \Rightarrow m_{H_2SO_4\left(dư\right)}=0,05.98=4,9\left(g\right)\)
b) \(n_{Fe_2\left(SO_4\right)_3}=n_{Fe_2O_3}=0,15\left(mol\right)\)
=> \(m_{Fe_2\left(SO_4\right)_3}=0,15.400=60\left(g\right)\)
c) \(V_{ddFe_2\left(SO_4\right)_3}=V_{ddH_2SO_4}=200\left(ml\right)=0,2\left(l\right)\)
Vậy: \(C_{MddFe_2\left(SO_4\right)_3}=\dfrac{0,15}{0,2}=0,75\left(M\right)\)
nFe2O3= 24/160 = 0,15 mol
nH2SO4 = 0,2.2,5= 0,5 mol
Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O
0,15 0,5
ta có 0,15/1 < 0,5/3
=> H2SO4 dư
Fe2O3 +3H2SO4 -> Fe2(SO4)3 +3H2O
0,15 0,45 0,15
nH2SO4 dư = 0,5-0,45=0,05mol
mH2SO4 dư = 05.98=4,9(g)
b, mFe2(SO4)3 = 0,15.400=60(g)
c, C(Fe2(SO4)3) = n/V = 0,15/ 0,2=0,75M
C(H2SO4) dư = n/V = 0,05/0,2= 0,25 M

Câu 1:
- Vì khi ở phòng kín lượng oxi càng ngày càng giảm vì cơ thể đã lấy để sử dụng và khí cacbonic càng nhiều vì cơ thể đã thải ra nên khi đông người thì không có đủ oxi để dùng nên thấy ngột ngạt
Câu 2: https://vn.answers.yahoo.com/question/index?qid=20100314041838AAz7o0e












1C
2A
3C
4B
5C
6D
7B
8A
9D
10C