Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\) - pư hóa hợp
b, \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\) - pư hóa hợp
c, \(3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\) - pư thế
d, \(SO_3+H_2O\rightarrow H_2SO_4\) - pư hóa hợp
e, \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\) - pư oxi hóa khử
f, \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\) - pư họa hợp
g, \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\) - pư phân hủy
h, \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\) - pư phân hủy
i, \(Fe+2HCl\rightarrow FeCl_2+H_2\) - pư thế
j, \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\) - pư thế

a) Fe2O3 + 3H2 → 2Fe + 3H2O (phản ứng thế)
b) SO3 + H2O → H2SO4 (phản ứng hoá hợp)
c) 2Al + Fe2O3 → 2Fe + Al2O3 (phản ứng thế)
d) CaO + H2O → Ca(OH)2 (phản ứng hoá hợp)
e) 2K + 2H2O → 2KOH + H2 (phản ứng thế)
f) Zn + H2SO4 → ZnSO4 + H2 (phản ứng thế)

Oxit tác dụng với nước: SO3, K2O, CaO, P2O5
- SO3 + H2O --> H2SO4
- K2O + H2O --> 2KOH
- CaO + H2O --> Ca(OH)2
P2O5 + 3H2O --> 2H3PO4
Không được nha cậu ơiii, chỉ có các oxit tan trong nước mới phản ứng được với nước thui, CuO với Al2O3 k phản ứng đc. Với lại CO đâu có tác dụng đc với nước âu

a) mCaCO3 = mCaO + mCO2
b) Khối lượng của CaCO3 đã phản ứng:
140 + 110 = 250 kg
Tỉ lệ phần trăm khối lượng CaCO3 chứa trong đá vôi:
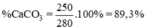

\(a,4P+5O_2\xrightarrow{t^o}2P_2O_5\\ b,Fe_3O_4+4H_2\to 3Fe+4H_2O\\ c,3Ca+2H_3PO_4\to Ca_3(PO_4)_2+3H_2\\ d,CaCO_3+2HCl\to CaCl_2+H_2O+CO_2\uparrow\\ e,Zn+2HCl\to ZnCl_2+H_2\\ f,MgCl_2+Na_2CO_3\to MgCO_3\downarrow+2NaCl\\ g,Fe+CuSO_4\to FeSO_4+Cu\\ h,CO_2+Ca(OH)_2\to CaCO_3\downarrow+H_2O\)

a) Phương trình phản ứng:
CO2 + H2O → H2CO3 (1).
SO2 + H2O → H2SO3 (2).
Zn + 2HCl → ZnCl2 + H2 (3).
P2O5 + 3H2O → 2H3PO4 (4).
PbO + H2 → Pb + H2O (5).
b) - Phản ứng (1), (2) và (4) là phản ứng kết hợp vì một chất mới tạo từ nhiều chất.
- Phản ứng (3) và (5) là phản ứng thế và đồng thời phản ứng (5) là phản ứng oxi hóa khử.

a)\(CuO+H_2\xrightarrow[]{t^0}Cu+H_2O\)
- Phản ứng thế
b)\(CaO+H_2O\xrightarrow[]{}Ca\left(OH\right)_2\)
-Phản ứng hoá hợp
c)\(Al_2O_3+3H_2O\xrightarrow[]{}2Al\left(OH\right)_3\)
-Phản ứng hoá hợp
d)\(P_2O_5+3H_2O\xrightarrow[]{}2H_3PO_4\)
-Phản ứng hoá hợp
e)\(CaO+CO_2\xrightarrow[]{}CaCO_3\)
-Phản ứng hoá hợp
f)\(Na_2O+H_2O\xrightarrow[]{}2NaOH\)
-Phản ứng hoá hợp
g)\(2SO_2+O_2\xrightarrow[]{t^0}2SO_3\)
-Phản ứng hoá hợp
h)\(CuO+H_2O\xrightarrow[]{}Cu\left(OH\right)_2\)
-Phản ứng hoá hợp
a) 4P + 5O2 \(\underrightarrow{t^o}\) 2P2O5 ( pứ hóa hợp)
b) H2 + FeO \(\underrightarrow{t^o}\) Fe + H2O ( pứ OXHK , pứ thế)
c) SO3 + H2O \(\rightarrow\) H2SO4 ( pứ hóa hợp )
d) BaO + H2O \(\rightarrow\) Ba(OH)2 ( pứ hóa hợp )
CaCO3 \(\underrightarrow{t^o}\) CaO + CO2\(\uparrow\) ( pứ phân hủy )
a, P + O2 -) P2O5
c, SO3 + H2O-) H2SO4
d BaO + H2O -) Ba ( OH)2
e, CaCO3 -) Cao + CO2
cau b mik chuaa hieu lam