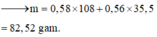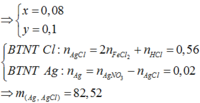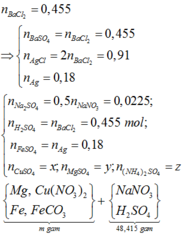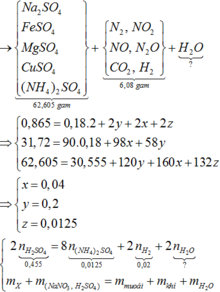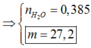Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Trong các sản phẩm khử có H2 nên NO3- hết
Sau khi tác dụng với NaOH thì dung dịch thu được chỉ gồm NaCl là KCl
→ nHCl = nNaCl + nKCl = nNaOH + nKNO3 = 0,9mol
Bảo toàn H có nHCl = 2nH2 + 4nNH4 + 2nH2O
→ nH2O = 0,4 mol
BTKL : mA + mHCl + mKNO3 = mmuối + mH2O + mC
→ mA = 20,6 gam
Đặt a, b,c, d lần lượt là số mol của Mg, MgCO3, Fe, Fe(NO3)2
Có mA = 24a + 84b + 56c + 180d =20,6
nO = 3b+ 6d = 20,6. %O : 16 = 0,48
mmuối = 24(a+b) + 56(c + d ) + 0,07.39 + 0,01.18 + 0,09.35,5 = 45,74
moxit = 40 (a +b ) + 160 (c + d ) . ½ = 17,6
Giải hệ được a =0,26; b = 0,1; c= 0,01; d=0,03
→ %Fe = 2,7 %

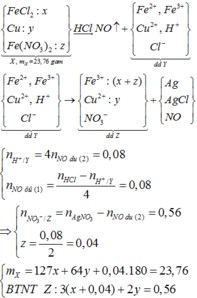
Do Y tác dụng AgNO3 sinh ra NO ⇒ trong Y có chứa H+ và NO3– hết.
4H+ + NO3– + 3e → NO + 2H2O ⇒ ở phản ứng đầu, nH+ = 0,4 – 0,02 × 4 = 0,32 mol.
⇒ nNO3– = 0,32 ÷ 4 = 0,08 mol ⇒ nFe(NO3)2 = 0,04 mol.
Đặt nFeCl2 = x mol; nCu = y mol. mX = 127x + 64y + 0,04 × 180 = 23,76 gam.
Bảo toàn nguyên tố Clo : nAgCl = 2x + 0,4 mol.
Bảo toàn nguyên tố Ag : nAg = 0,58 – (2x + 0,4) = 0,18 – 2x mol.
Bảo toàn electron cả quá trình : nFeCl2 + 2nCu + nFe(NO3)2 = nAg + 3/4nH+.
⇒ x + 2y + 0,04 = 0,18 – 2x + 3/4 × 0,4 ⇒ giải: x = 0,08 mol; y = 0,1 mol.
⇒ nAg = 0,02 mol; nAgCl = 0,56 mol ⇒ m = 0,02 × 108 + 0,56 × 143,5 = 82,52
Đáp án A

Đáp án C
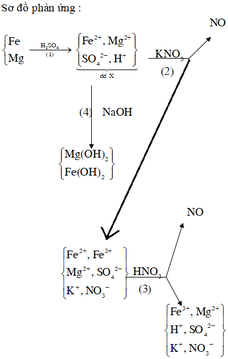
Hết 0,12 mol NaOH mới có kết tủa chứng tỏ Y có H+. Vậy n(H+) = 0,12 mol
Chất rắn thu được khi cho tác dụng với NaOH là Fe(OH)2 và Fe(OH)3. (Nếu xét chỉ có Fe(OH)2 hay chỉ có Fe(OH)3 thì khối lượng rắn thu được không thỏa mãn)
Y có H+ , có Fe2+ nên NO3- hết.
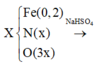
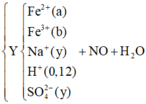
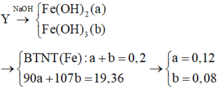
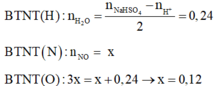
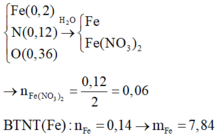

Đáp án C
Xét toàn bộ quá trình: với 0,4 mol HC1 và lượng NO 3 - dư thừa thì sinh được 0,1 mol NO.
Mà lúc sau ra 0,02 mol chứng tỏ X + HC1 sẽ cho 0,08 mol NO.
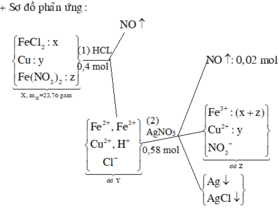
Theo đó, bảo toàn nguyên tố N → X có 0,04 mol Fe(NO3)2. Xem xét quá trình:
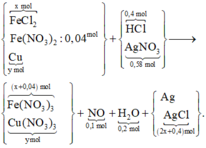
Gọi số mol, suy luận và "ban bật" nhanh các số liệu cơ bản như sơ đồ trên.
Lập ngay hệ phương trình:
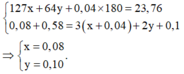
(Đây là hệ các phương trình về khối lượng và bảo toàn nguyên tố N).
Thay ngược lại, có m gam kết tủa gồm 0,58 mol Ag và 0,56 mol Cl (về mặt nguyên tố).