Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.BT\left[Cl\right]:n_{AgCl}=n_{HCl\left(X\right)}=\dfrac{35,875}{143,5}=0,25mol\\ HCl+NaOH->NaCl+H_2O\\ n_{HCl\left(Y\right)}=0,5.0,3=0,15mol\\ C_{M\left(Z\right)}=\dfrac{0,4}{2}=0,2\left(M\right)\\ b.Fe+2HCl->FeCl_2+H_2\\ n_{HCl\left(X\right)}=a;n_{HCl\left(Y\right)}=b\left(mol\right)\\ a-b=\dfrac{0,448}{22,4}.2=0,04mol\\ Từ\left(a\right)\Rightarrow n_{HCl\left(X\right)}:n_{HCl\left(Y\right)}=0,25:0,15=\dfrac{5}{3}=\dfrac{a}{b}\\ \Rightarrow a=0,1;b=0,06\\ C_{M\left(X\right)}=\dfrac{0,1}{0,1}=1M\\ C_{M\left(Y\right)}=\dfrac{0,06}{0,1}=0,6\left(M\right)\)

-khi trộn dung dịch A và B cùng là HCl thì vẫn được dung dịch HCl
mC= mA + mB = 7,3 + 58,4 =65,7(g)
nC = 65,7/36,5=1,8 (mol)
M(C) = 1,8/3= 0,6 (M)
-ta có : V1 + V2 =3 lít
=> V1 = 3-V2
lại có
M(B) - M(A) = (7.3/36,5)/V1 - (58,4/36,5)/V2 = 0,2/(3-V2) - 1,6/V2 =0,6
=> V2= căn 8
=> V1 = 3- căn 8

A: H2SO4 : CA (M)
B1: NaOH : C1 (M)
B2: NaOH: C2 (M)
TH1: VB1: VB2 = 1: 1 => gọi thể tích của mỗi chất là V
Nồng độ của NaOH sau khi trộn là: CM = n : V
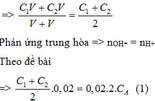
TH2: VB1 : VB2 = 2 : 1 => Đặt VB2 = V (lít) thì VB1 = 2V (lít)
Nồng độ của NaOH sau khi trộn là:

Ta có:
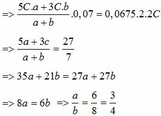

Ta có : C1=2C2
=> Gọi nH2SO4 =x
=> n HCl = 2x
Bảo toàn nguyên tố H :\(n_{HCl}.1+n_{H_2SO_4}.2=n_{H_2}.2\)
\(\Rightarrow2a+2a=\dfrac{13,44}{22,4}=0,6.2\)
=>a = 0,3(mol)
=> CMHCl = \(\dfrac{0,6}{0,3}=2M\); CMH2SO4 = \(\dfrac{0,3}{0,3}=1M\)
Dung dịch B gồm : Mg 2+ , Al3+ , Cl- , SO4 2-
\(n_{Cl^-}=n_{HCl}=0,6\left(mol\right);n_{SO_4^{2-}}=n_{H_2SO_4}=0,3\left(mol\right)\)
Bảo toàn điện tích cho dung dịch B:
\(n_{Mg}.2+n_{Al}.3=0,6+0,3.2\) (1)
Theo đề bài : \(24.n_{Mg}+27.n_{Al}=12,6\) (2)
Từ (1), (2)=> \(\left\{{}\begin{matrix}n_{Mg}=0,3\\n_{Al}=0,2\end{matrix}\right.\)
=> \(\%m_{Mg}=\dfrac{0,3.24}{12,6}.100=57,14\%\)
=> % m Al = 100 -57.14 = 42,86%

n(HCl) = 0,15 mol; n(CO2) = 0,1 mol.
+) Nếu NaOH dư thì dd X gồm Na2CO3 và NaOH.
BTNT(C): n(Na2CO3) = n(CO2) + n(CaCO3) = 0,1 + 0,15 = 0,25.
Để có khí thì lượng HCl phải lớn hơn số mol của NaOH và Na2CO3 cộng lại mà số mol HCl chỉ có 0,15 nên trường hợp này loại.
+) Vậy X gồm Na2CO3, NaHCO3.
Na2CO3 + HCl → NaHCO3 + NaCl. (1)
NaHCO3 + HCl → NaCl + CO2 + H2O. (2)
Nên n(Na2CO3) = n(HCl) – n(CO2) = 0,15 – 0,1 = 0,05.
BTNT (C): n(NaHCO3) = n(CO2) + n(CaCO3) – n(Na2CO3) = 0,1 + 0,15 – 0,05 = 0,2 mol.
BTĐT: n(OH) = 2.n(Na2CO3) + n(NaHCO3) = 2.0,05 + 0,2 = 0,3.
CM =a = 0,75M.
+) Bảo toàn C => \(n_{CO_2}=0,25\left(mol\right)\)
=>\(V=0,25.22,4=5,6\left(l\right)\)
CTV hay các thành viên cho em hỏi cái này của trương trình lớp 9 có phải ko ạ

nOH = nNaOH + 2nBa(OH)2 = 0,15 + 0,175 . 2 = 0,5 (mol)
nHCl = 2a (mol)
nH2SO4 = 0,1 . 2 = 0,2 (mol)
nH = nHCl + 2nH2SO4 = 2a + 2 . 0,2 = 2a + 0,4 (mol)
Để phản ứng trung hòa được thì nH = nOH
=> 0,5 = 0,4 + 2a
=> a = 0,05M

nHCl (X) = 0,15.C1 (mol)
nHCl (Y) = 0,5.C2 (mol)
nHCl (Z) = 0,15C1 + 0,5C2 (mol)
1/10 dung dịch Z có \(nHCL=\frac{0,15C_1+0,5C_2}{10}\)
Trung hòa 1/10 dd Z:
nNaOH = 1. 0,01 = 0,01 mol
nBa(OH)2 = 0,25 . 0,01 = 0,0025 mol
NaOH + HCl → NaCl + H2O
0,01__0,01
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
0,0025___0,005
\(n_{HCl}=\frac{0,15C_1+0,5C_2}{10}=0,01+0,005=0,015\left(mol\right)\)
\(\rightarrow C_2=0,3-0,3C_1\left(1\right)\)
Trộn V1 l dd X với V2 l dd Y:
\(V_1=\frac{0,05}{C_1}\left(l\right)\)
\(V_2=\frac{0,15}{C_2}\left(l\right)\)
\(V_1+V_2=1,1\)
\(\rightarrow\frac{0,05}{C_1}+\frac{0,15}{C_2}=1,1\left(2\right)\)
Thay (1) vào (2) → \(\left\{{}\begin{matrix}C_1=0,5\\C_2=\frac{1}{11}\end{matrix}\right.\)
TH1: C1 = 0,5 → C2 = 0,15
V1 = 0,1
V2 = 1
TH2:\(C_1=\frac{1}{11}\rightarrow C_2=\frac{3}{11}\)
Do C1>C2 → LOẠI