Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : C
Y không thể là CO32- vì sẽ kết tủa Mg2+ => Y2- là SO42-
Bảo toàn điện tích : nK + 2nMg + nNa = nCl + 2nSO4
=> nSO4 = 0,6 mol
=> m = 111,9g

Bảo toàn điện tích và bảo toàn khối lượng:
0,1.1 + 0,2.2 + 0,1.1 = 0,2.1+ a.2 => a = 0,2.
Mà muốn dung dịch tồn tại được thì các ion không được phản ứng với nhau. Do đó Y2- chỉ có thể là SO42-(theo đáp án)
m = 0,1.39 + 0,2.24 + 0,1.23 + 0,2.35,5 + 0,2.96 = 37,3 gam.
=> Đáp án D

Chọn B.
Bảo toàn điện tích: ![]()
Tương đương: 3.0,2 + 2.0,25 = 2a + 0,5 ⇒ a = 0,3 mol.
Bảo toàn khối lượng: mmuối = 0,2.27 + 0,3.96 + 0,25.24 + 0,5.35,5 = 57,95 gam.

Đáp án : C
Bảo toàn điện tích trong dung dịch: nY = 0,1 + 0,2. 2 + 0,1 – 0,2 = 0,4 mol
Đáp số cho ta hai ion Y- là và , nhưng loại vì nó không thể tồn tại trong cùng 1 dung dịch với ion
mmuối = 0,1. 39 + 0,2. 24 + 0,1. 23 + 0,2. 35,5 + 0,4. 62 = 42,9 g

Chọn D
BTĐT: nNO3- = nNa+ + 2nBa2+ + 2nMg2+ - nCl- = 0,3.1+0,1.2+0,05.2-0,2.1=0,4 mol
m muối = mNa+ + mBa2+ + mMg2+ + mCl- + mNO3-
= 0,3.23+0,1.137+0,05.24+0,2.35,5+0,4.62 = 53,7 gam
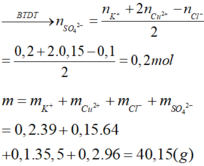
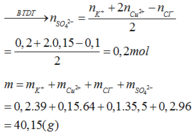

Chọn C
Loại B, C vì CO32- tạo kết tủa với Mg2+. Như vậy Y2- là SO42-.
Bảo toàn điện tích ⇒ 0,3 + 0,6.2 + 0,3 = 0,6 + 2a ⇒ a = 0,6
⇒ m = 0,3.39 + 0,6.24 + 0,3.23 + 0,6.35,5 + 0,6.96 = 111,9