
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

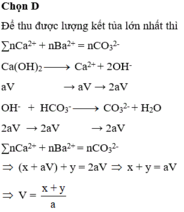

Đáp án : C
Vì Mg và Zn đều có hóa trị 2 nên gọi kí hiệu chung là M
Trước tiên có phương trình ion cho phản ứng với HNO3 như sau
(3b + 8c)/2 M + (b + 2c)N+5 -> (3b + 8c)/2M+2 + bN+2 + 2cN+1
số mol M là (3b + 8c)/2 và số mol HNO3 pư là (b + 2c + 3b + 8c) = 4b + 10c
=> Số mol HNO3 dư là (a – 4b – 10c) mol
Để lượng kết tủa lớn nhất thì NaOH trung hòa hết HNO3 và phần dư có tỉ lệ 2 : 1 với M(NO3)2
=>Số mol NaOH là V = (a - 4b - 10c) + 2.(3b + 8c)/2 = a - b – 2c

Chọn đáp án A
BTĐT Þ nMg2+ = 1/2 + 2 = 2,5 Þ nNa2CO3 cần = 2,5 Þ V = 2,5/2 = 1,25.

Đáp án A
nOH- = 0,1.2 + 0,225 + 0,2 = 0,625 mol
Do nH+>nCO2 nên X có cả CO32- => X không có Ba2+ => nBaCO3 = 0,1 mol
Đặt x, y là số mol CO32- và số mol HCO3- phản ứng với H+
x+y = nCO2 = 0,25
2x+y = nH+ = 0,35
=> x = 0,1; y = 0,15
Dung dịch X chứa: K+ (0,225 mol), Na+ (0,2 mol), CO32- (0,1k mol), HCO3- (0,15k mol)
BTĐT: 0,225 + 0,2 = 2.0,1k + 0,15k => k = 1,3
BTNT C: nCO2 ban đầu = nBaCO3 + nCO32- + nHCO3- = 0,1 + 0,13 + 0,195 = 0,425 mol
=> V = 9,52 lít