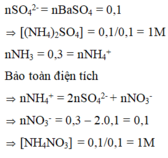Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Dùng Ba(NO3)2 thì:
CO32-+ Ba2+ → BaCO3 ↓
2PO43- + 3Ba2+→ Ba3(PO4)2
SO42-+ Ba2+ → BaSO4
Khi đó trong dung dịch chỉ còn anion NO3-

Đáp án D
nNH4+ = nNH3 = 0,02
Nếu cho dung dịch A tác dụng với dung dịch H2SO4 loãng, dư thì thu được 0,224 lít khí (đktc) ⇒ nCO32- = nCO2 = 0,01
mBaCO3 + mBaSO4 = 4,3 ⇒ nSO42- = 0,01
⇒ nNa+ = 0,02 ⇒ m = m Na+ + m NH4+ + m CO32- + m SO42- = 2,38g

Đáp án C
Gọi số mol mỗi ion NH4+, Na+, CO32-, SO42- trong mỗi phần lần lượt là x, y, z , t mol
Phần 1: Ba2++ CO32-→ BaCO3
z z
Ba2++ SO42- → BaSO4
t t
NH4++ OH-→ NH3+ H2O
x x = PV/RT= 0,02 mol
mkết tủa = mBaCO3+ mBaSO4 = 197z+233t = 4,3 suy ra t = 0,01 mol
Phần 2: 2H++ CO32- → CO2+ H2O
z mol z mol = 0,01
Định luật bảo toàn điện tích: x+y = 2z+ 2t suy ra y = 0,02 mol
mmuối = (18x+ 23y+60z+96t).2 = 4,76 gam

Đáp án B
Để dung dịch tồn tại thì các ion không phản ứng với nhau và định luật bảo toàn được thỏa mãn. Ở đây chỉ có đáp án B thỏa mãn.

Đáp án A
Các ion cùng tồn tại trong 1 dung dịch là: (a), (i) vì các ion này không phản ứng tạo kết tủa.

Đáp án B
Ba2++ SO42- →BaSO4
0,1 ← 23,3/233
NH4++ OH- →NH3+ H2O
0,3← 0,3
Theo ĐLBT ĐT thì: nNO3(-)=0,1 mol
Vậy dung dịch X có 0,1 mol (NH4)2SO4 và 0,1 mol NH4NO3
Suy ra nồng độ mol (NH4)2SO4 1M và NH4NO3 1M

Đáp án B
Loại ngay A và D do H+ và CO32- không tồn tại trong cùng 1 dung dịch
Xét B: nK+ + nNH4+ = 0,15 + 0,25 = 0,4 mol; nCl- + 2nCO32- = 0,1 + 2.0,15 = 0,4 mol
=> thỏa mãn định luật bảo toàn điện tích
Xét C: nK+ + 2nMg2+ = 0,15 + 2.0,1 = 0,35 mol; nCl- + 2nSO42- = 0,1 + 2.0,075 = 0,25 mol
=> không thỏa mãn định luật bảo toàn điện tích