

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Chọn A.
Hỗn hợp khí gồm
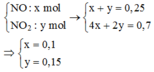
→ B T : e n F e p ư = 3 n N O + n N O 2 2 = 0 , 225 m o l ⇒ m - 0 , 75 m = 0 , 225 . 56 ⇒ m = 50 , 4 g

Đáp án A
Các phản ứng:
Do Fe chiếm 30% về khối lượng mà sau phản ứng còn 0,75m tức phản ứng 25%. Fe có tính khử mạnh hơn Cu nên Fe sẽ phản ứng trước. Do đó kim loại Fe dư
=> Muối thu được là muối Fe(NO3)2
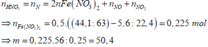

Đáp án C
Ta có nN2O = 0,1 mol; nNO = 0,2 mol và nNO2 = 0,3 mol
Có mmuối = mkl + mNO3- = 100 + 62. ( 0,1. 8 + 0,2. 3+ 0,3) = 205,4 gam
Có nHNO3 pư = 0,1.10 + 0,2. 4 + 0.3.2 = 2,4 mol

Đáp án D
Quan sát quá trình 1:

BTKL có nH2O = 0,92 mol. Bảo toàn H chứng
tỏ trong X chứa 0,26 mol H+ dư như trên.
♦ Quá trình 2: để ý khí Y có M = 18,8
→ là H2 và NO. Quan sát quá trình chính:
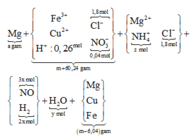
giải tỉ khối Y tìm tỉ lệ 2 khí NO : H2 là 3 : 2 rồi gọi các ẩn như sơ đồ:
• Ghép cụm: nH2O = 2nNO + 3nNH4 ⇄ y = 6x + 3z (1).
• bảo toàn nguyên tố N có: 3x + z = 0,04 mol (2).
• Bảo toàn nguyên tố H có: 4x + 2y + 4z = 0,26 mol (3)
Giải x = 0,01 mol; y = 0,09 mol; z = 0,01 mol ||→ bảo toàn điện tích có nMg2+ = 0,895 mol.
► Chỉ cần BTKL cả sơ đồ có ngay và luôn giá trị yêu cầu a = 21,84 gam