Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nitơ chiếm 80% thể tích không khí, điều đó có nghĩa là trong không khí mỗi khi có 1 mol oxi sẽ có 4 mol nitơ.
S + O 2 → S O 2
Khi tạo thành 1 mol S O 2 hì hỗn hợp thu được gồm 1 mol S O 2 và 4 mol N 2
![]()
Tỉ khối của hỗn hợp đối với He là : d = 35,2/4 = 8,8

Đáp án B.
Bảo toàn khối lượng:
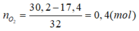
=> V = 0,4.22,4 = 8,96 (lít)

a)
$Fe + H_2SO_4 \to FeSO_4 + H_2$
Theo PTHH :
$n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$m_{Fe} = 0,15.56 = 8,4(gam)$
b)
$n_{H_2SO_4} = n_{H_2} = 0,15(mol)$
$C_{M_{H_2SO_4}} = \dfrac{0,15}{0,05} = 3M$
c)
$n_{FeSO_4} = n_{H_2} = 0,15(mol)$
$C_{M_{FeSO_4}} = \dfrac{0,15}{0,05} = 3M$

\(n_{Br_2}=0,3.2,5=0,75\left(mol\right)\)
PTHH: SO2 + 2H2O + Br2 ---> H2SO4 + 2HBr
0,75<------------0,75
MA = 1,6.28 = 44,8 (g/mol)
O2 dư tác dụng với S thì sau phản ứng chứa O2 và SO2
Áp dụng sơ đồ đường chéo đối với A:
\(\dfrac{n_{SO_2}}{n_{O_2}}=\dfrac{V_{SO_2}}{V_{O_2}}=\dfrac{44,8-32}{64-44,8}=\dfrac{2}{3}\)
\(\rightarrow n_{O_2}=\dfrac{3}{2}.0,75=1,125\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,75<-0,75<-----0,75
=> \(\left\{{}\begin{matrix}m=0,75.32=24\left(g\right)\\V=\left(1,125+0,75\right).22,4=42\left(l\right)\end{matrix}\right.\)

\(M_X = 18.2 = 36(đvC)\)
X gồm CO2,CO
Ta có :
\(44n_{CO_2} + 28n_{CO} = 36(n_{CO_2} + n_{CO})\\ \Rightarrow 8n_{CO_2} = 8n_{CO}\\ \Rightarrow n_{CO_2} = n_{CO}\)
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\)
Theo PTHH :
\(n_{CO} = n_{CO_2} = n_{CaCO_3} = \dfrac{20}{100} = 0,2(mol)\)
\(C + O_2 \xrightarrow{t^o} CO_2\\ 2C + O_2 \xrightarrow{t^o} 2CO\\ n_{O_2} = n_{CO_2} + \dfrac{n_{CO}}{2} = 0,3(mol)\\ \Rightarrow V = 0,3.22,4 = 6,72(lít)\)
\(\)

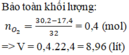



chữ mờ khó thấy ghê