Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

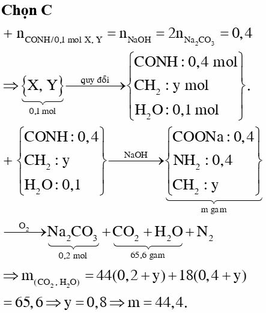
n(Na2CO3) = 0,2 → nmuối = 0,4
2 CnH2nO2NNa + (3n – 1,5) O2 → Na2CO3 + (2n – 1) CO2 + 2n H2O + N2
n(CO2) = 0,2(2n – 1)
n(H2O) = 0,4n
m(CO2) + m(H2O) = 65,6 → n = 3
→ m(CnH2nO2Nna) = 44,4 gam
n(O2) = 1,5
Bảo toàn khối lượng cho phản ứng thủy phân E:
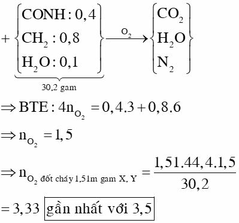
m(E) + 40.0,4 = 44,4 + 0,1.18 → m(E) = 30,2
Đốt 30,2 gam E cần 1,5 mol O2
→ Đốt 1,51.44,4 gam E cần 3,33 mol O2
→ Đáp án C

Chọn đáp án B
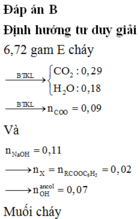
Giải đốt cháy: giả thiết mCO2 + mH2O = 87,6 gam.
Tương quan: ∑nCO2 – ∑nH2O = 0.nX + 2.nY = 0,3 mol.
||→ giải ra: nCO2 = 1,5 mol và nH2O = 1,2 mol.
||→ số Ctrung bình = 2. vì yêu cầu m ≥ 4 → n = 1. 0,6m + 0,15n = 1,5 → m = 6.
Chú ý thêm E + NaOH → 2 muối + 1 ancol, X là HCOOH, mancol < 9,3 gam.
một số nhóm cố định: 2C cho –COO (2 chức este); 2C cho nối đôi C=C,
còn lại 2C cho các gốc hiđrocacbon, tổng kết các dữ kiện trên
||→ Y phải là HCOOCH2-CH2-OOCCH=CH2 (este của etilen glicol với axit fomic và acrylic).
Chọn đáp án B. ♦.
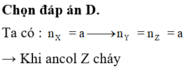
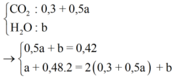
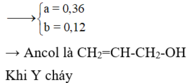
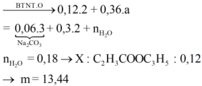


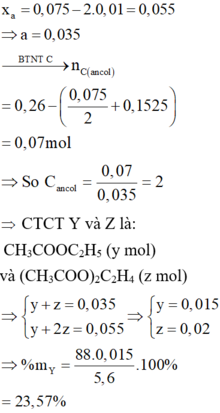



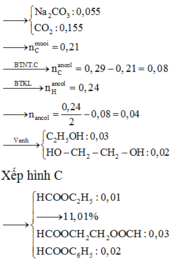
Chọn đáp án A
nCO2 = nO2 ⇒ X có dạng của cacbohidrat Cn(H2O)m hay CnH2mOm.
Số nhóm chức este = m ÷ 2 ||► Este X no, hở ⇒ k = πC=O = 0,5m.
● số H = 2 × số C + 2 – 2k ⇒ 2m = 2n + 2 – m.
Lại có: mCO2 = 3,055.mH2O ⇒ nCO2 = 1,25.nH2O ⇒ n = 1,25m
Giải hệ có: n = 5; m = 4 ⇒ C5H8O4 ⇒ nX = 0,12 mol.
nNaOH = 0,12 × 2 = 0,24 mol. Bảo toàn khối lượng: mY = 7,44(g).
► Gọi n là số nhóm chức của Y ⇒ nY = 0,24 ÷ n ⇒ MY = 31n.
⇒ n = 2; MY = 62 ⇒ Y là C2H4(OH)2.