Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nCH4 = 2.24/22.4 = 0.1 (mol)
CH4 + 2O2 -to-> CO2 + 2H2O
0.1____0.2______0.1
VO2 = 0.2*22.4 = 4.48 (l)
VCO2 = 0.1*22.4=2.24 (l)

\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\Rightarrow n_{CO_2}=n_{CH_4}=0,5\left(mol\right);n_{O_2}=2.n_{CH_4}=2.0,5=1\left(mol\right)\\ V_{O_2\left(đktc\right)}=n_{O_2}.22,4=1.22,4=22,4\left(l\right)\\ V_{CO_2\left(đktc\right)}=n_{CO_2}.22,4=0,5.22,4=11,2\left(l\right)\)

\(n_{CH_4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,25-->0,5-------->0,25
=> \(V_{O_2}=0,5.22,4=11,2\left(l\right)\)
\(V_{CO_2}=0,25.22,4=5,6\left(l\right)\)

a) Những khí tác dụng với nhaư từng đôi một là:
CH4 và O2; CH4 và Cl2; H2 và O2; H2 và Cl2.
b) Những hỗn hợp nổ là những hỗn hợp khi phản ứng tỏa nhiều nhiệt, đó là các hỗn hợp: CH4 và O2; H2 và O2

1)
$CH_4 +2 O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
Theo PTHH :
$V_{O_2\ cần\ dùng} = 2V_{CH_4} = 24,79(lít)$
$V_{CO_2} = V_{CH_4} = 12,395(lít)$
2)
a)
$C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O$
$V_{O_2} = 3V_{C_2H_4} = 14,874(lít)$
b) $V_{không\ khí} = V_{O_2} : 20\% = 14,874 : 20\% = 74,37(lít)$

\(n_{C_2H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{^{t^0}}2CO_2+H_2O\)
\(0.1........0.25...........0.2\)
\(V_{O_2}=0.25\cdot22.4=5.6\left(l\right)\)
\(V_{CO_2}=0.2\cdot22.4=4.48\left(l\right)\)

\(n_{CH_4}=\dfrac{2,24}{22,4}=0,1mol\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
0,1 0,2 0,1
\(V_{O_2}=0,2\cdot22,4=4,48l\)
\(V_{CO_2}=0,1\cdot22,4=2,24l\)

\(n_{C_2H_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ a,2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\\ b,n_{CO_2}=0,125.2=0,25\left(mol\right)\\ m_{CO_2}=0,25.44=11\left(g\right)\\ c,n_{O_2}=\dfrac{5}{2}.0,125=0,3125\left(mol\right)\\ V_{O_2\left(đktc\right)}=0,3125.22,4=7\left(l\right)\\ \Rightarrow V_{kk\left(đktc\right)}=\dfrac{100}{20}.7=35\left(l\right)\)
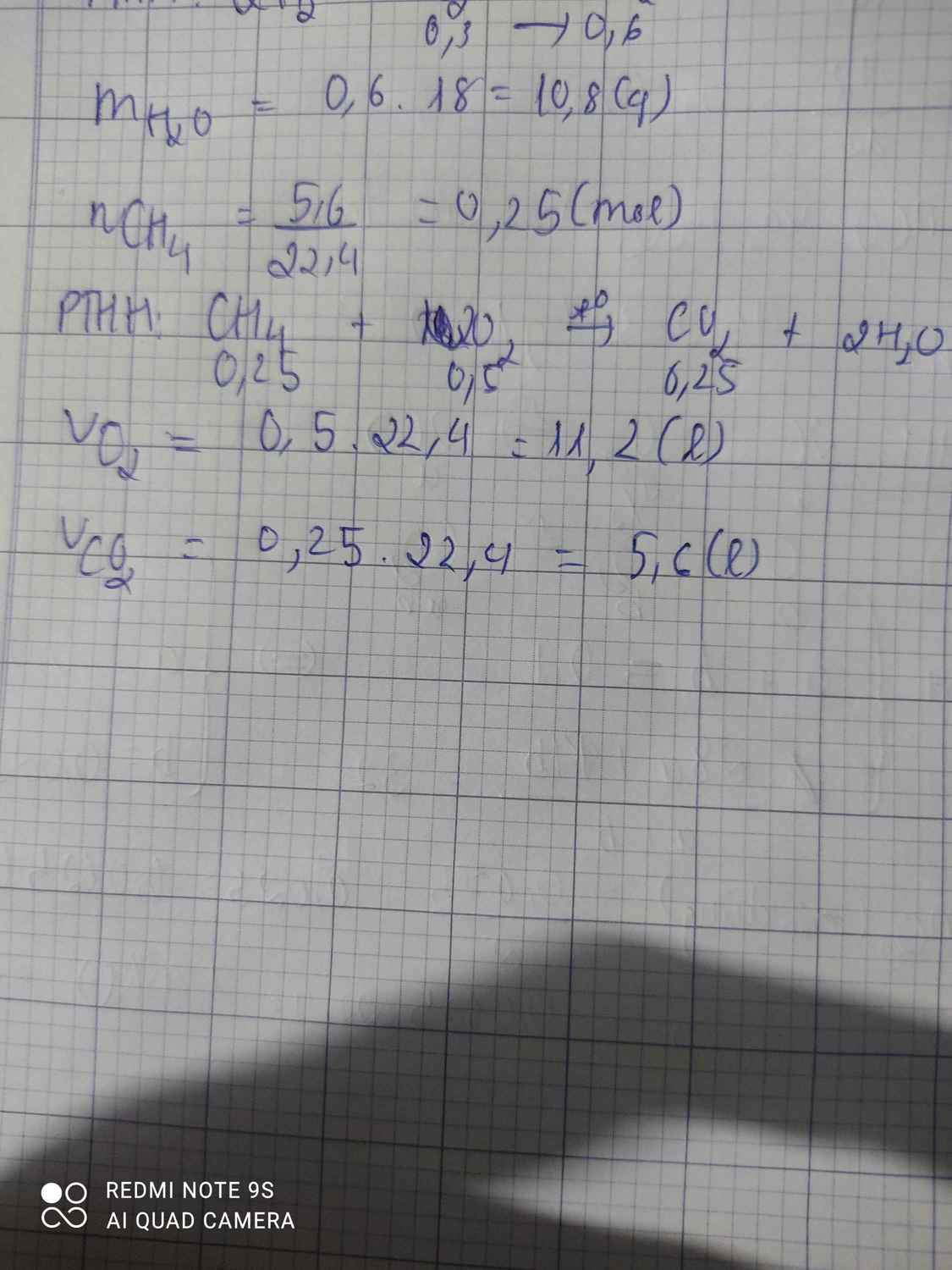
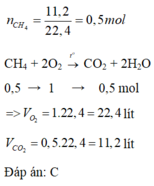
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
0.15 0.3 0.15
\(n_{CH_4}=\dfrac{3.36}{22.4}=0.15mol\)
\(V_{O_2}=0.3\times22.4=6.72l\)
\(V_{CO_2}=0.15\times22.4=3.36l\)