Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
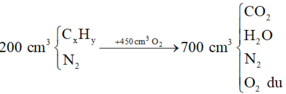
Quan sát 4 đáp án ta có công thức của X có dạng CxHy
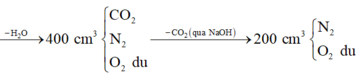
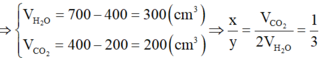
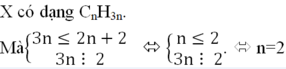
![]()

\(n_{N_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(n_{H_2O}=\dfrac{4,5}{18}=0,25\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
_______________0,2<------0,2________________(mol)
=> nCO2 = 0,2 (mol)
Bảo toàn C: nC(X) = 0,2 (mol)
Bảo toàn H: nH(X) = 2.0,25 = 0,5 (mol)
Bảo toàn N: nN(X) = 2.0,05 = 0,1 (mol)
=> \(n_O=\dfrac{7,5-0,2.12-0,5.1-0,1.14}{16}=0,2\left(mol\right)\)
=> nC : nH : nO : nN = 0,2 : 0,5 : 0,2 : 0,1 = 2:5:2:1
=> CTPT: (C2H5O2N)n

Gọi công thức phân tử của X là CxHyOz .
Sản phẩm cháy gồm CO2 và H2O.
Ở lần thí nghiệm thứ nhất, bình 1 chứa H2SO4 đậm đặc dư hấp thụ H2O và bình 2 chứa dung dịch nước vôi trong dư hấp thụ CO2.
Ở lần thí nghiệm thứ hai, bình 1 chứa CaO dư hấp thụ CO2 và toàn bộ hơi nước, bình 2 chứa P2O5 dư không hấp thụ gì vì toàn bộ lượng khí đã được hấp thụ ở bình 1. Do đó m2 = 0. Theo định luật bảo toàn khối lượng ta có
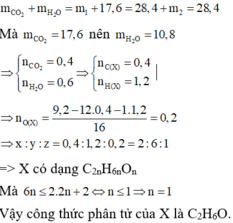

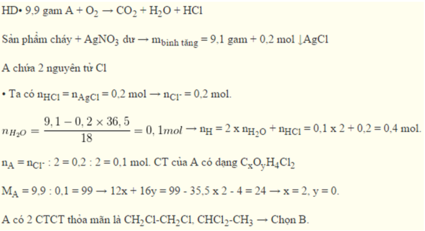

Đổi 10 cm3=10 ml,50cm3=50ml,70cm3=70ml,20cm3=20ml.Sản phẩm sau khi đốt cháy và ngưng tụ hơi nước có thể tích =50ml bao gồm:CO2,O2 dư,sau khi dẫn sản phẩm qua dung dịch kiềm dư thì CO2 được hấp thu vào trong dung dịch kiềm còn 20ml khí thoát ra là thể tích O2 dư=>VCO2 thu được sau khi đốt cháy=50-20=30(ml) và thể tích oxi phản ứng=70-20=50 ml.ta có pt: CxHy +(x+y/4)--->xCO2+y/2 H2O (1)
10ml--------------->x.10ml---->y/2.10ml
lại có VCO2=30=10.x=>x=3,bảo toàn nguyên tố Oxi ta có VO pu=VO(CO2)+VO(H2O)=2.VCO2+VH2O=>VH2O=50.2-30.2=40ml,lại có VH2O=y/2.10=40=>y=8
=> CTPT của X là C3H8.